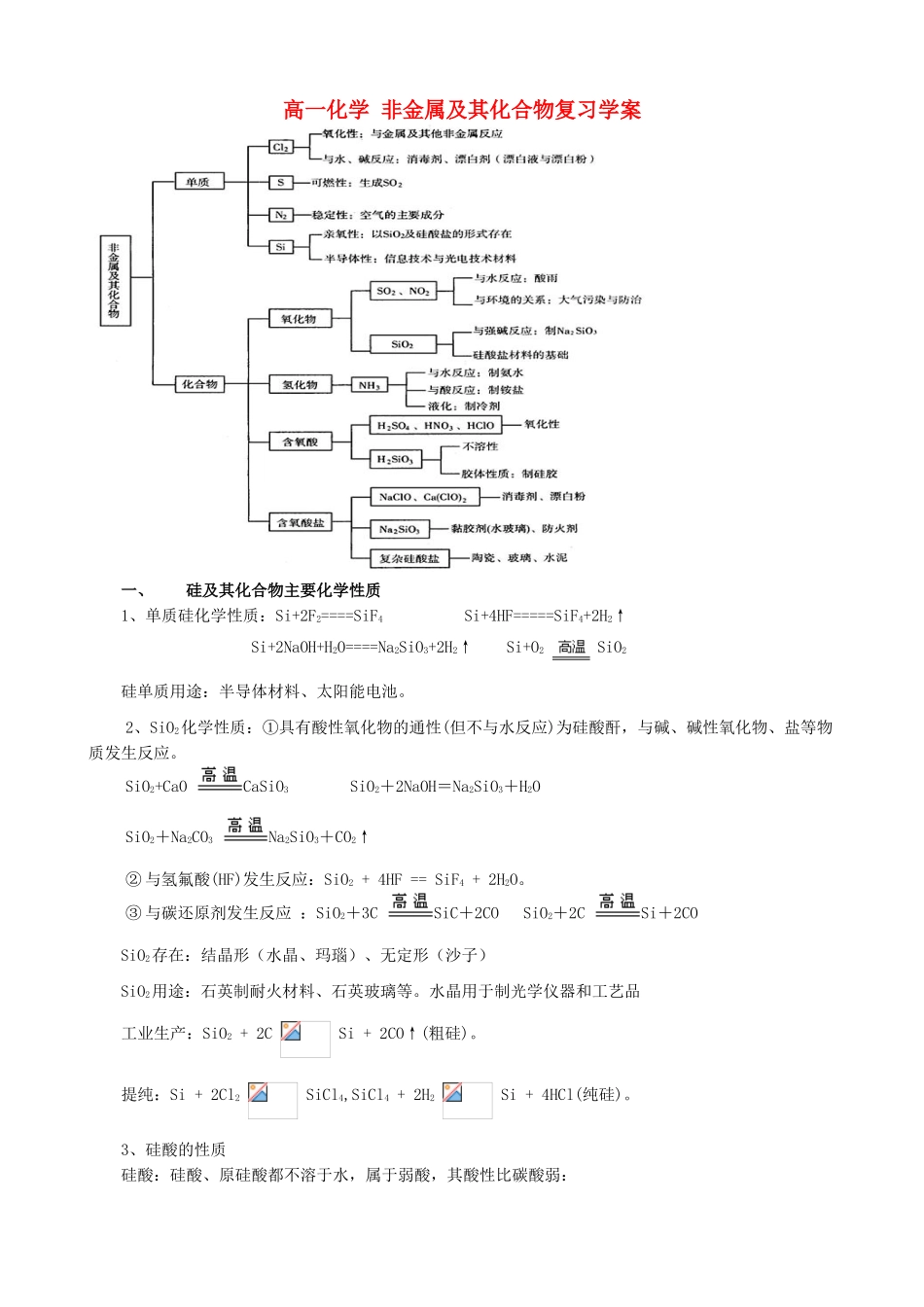
高一化学非金属及其化合物复习学案一、硅及其化合物主要化学性质1、单质硅化学性质:Si+2F2====SiF4Si+4HF=====SiF4+2H2↑Si+2NaOH+H2O====Na2SiO3+2H2↑Si+O2SiO2硅单质用途:半导体材料、太阳能电池
2、SiO2化学性质:①具有酸性氧化物的通性(但不与水反应)为硅酸酐,与碱、碱性氧化物、盐等物质发生反应
SiO2+CaOCaSiO3SiO2+2NaOH=Na2SiO3+H2OSiO2+Na2CO3Na2SiO3+CO2↑②与氢氟酸(HF)发生反应:SiO2+4HF==SiF4+2H2O
③与碳还原剂发生反应:SiO2+3CSiC+2COSiO2+2CSi+2COSiO2存在:结晶形(水晶、玛瑙)、无定形(沙子)SiO2用途:石英制耐火材料、石英玻璃等
水晶用于制光学仪器和工艺品工业生产:SiO2+2CSi+2CO↑(粗硅)
提纯:Si+2Cl2SiCl4,SiCl4+2H2Si+4HCl(纯硅)
3、硅酸的性质硅酸:硅酸、原硅酸都不溶于水,属于弱酸,其酸性比碳酸弱:Na2SiO3+2HCl+H2O=2NaCl+H4SiO4↓H4SiO4===H2SiO3+H2O(易)Na2SiO3+CO2+H2O=Na2CO3+H2SiO4↓4、硅酸钠(Na2SiO3):水溶液称之为水玻璃或泡花碱,粘合剂、防腐剂
制取:SiO2+2NaOH=Na2SiO3+H2O主要性质:Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3Na2SiO3+2HCl=H2SiO3(胶体)+2NaCl硅酸盐产品:水泥(3CaO·SiO22CaO·SiO23CaO·Al2O3)、玻璃(Na2O·CaO·6SiO2)、陶瓷
二、氯及其化合物主要化学性质1、氯气的化学性质:2Na+Cl22NaClCu+Cl2CuCl22Fe+3Cl22FeCl3Cl