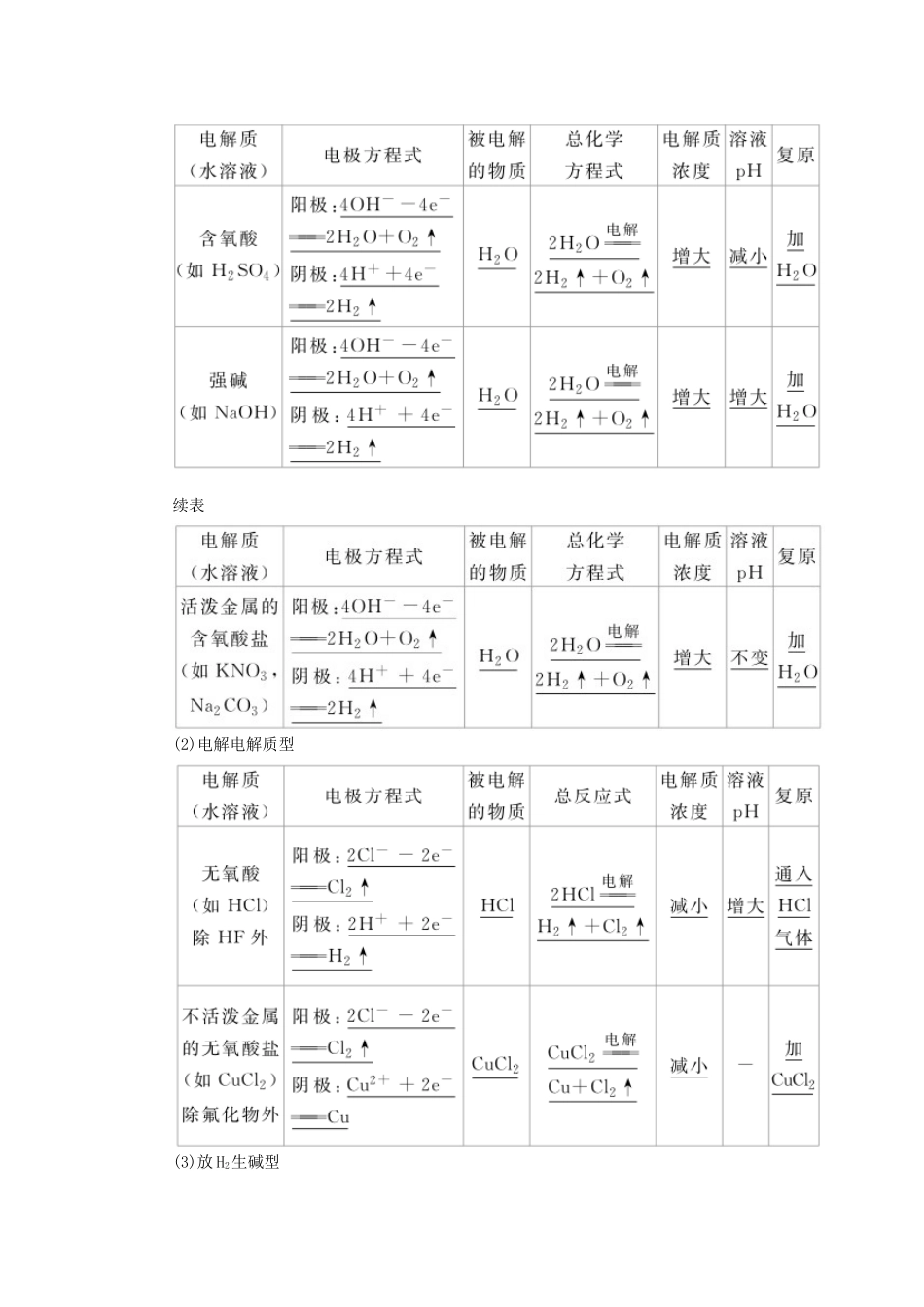
电解池金属的电化学腐蚀与防护明考纲1.了解电解池的工作原理,并能写出电极反应及总反应的方程式。2.掌握电解原理的应用如氯碱工业、电镀、电解精炼等。3.理解金属发生电化学腐蚀的原因,金属腐蚀的危害,防止金属腐蚀的措施。析考情电解原理的考查一是在选择题中出现:①新型充电电池充电时的分析及电极方程式的判断,②电解原理在工业生产中的应用;二是在填空题中出现:①考查电解过程的分析,多借助于图象考查考生的分析能力及离子放电顺序,②新情境下考查电极反应式的书写,需要借助于题给信息进行分析,考查考生的信息获取、理解、应用能力。考点电解原理1.电解(1)定义:使电流通过电解质溶液(或熔融的电解质)而在阴、阳两极引起氧化还原反应的过程。在此过程中,电能转化为化学能。(2)特点:①电解是不可逆的;②电解质导电一定发生化学变化。2.电解池(1)概念:电解池是把电能转化为化学能的装置。(2)电解池的构成条件①有与电源相连的两个电极。②两个电极插入电解质溶液(或熔融电解质)中。③形成闭合回路。(3)电极名称及电极反应式以用惰性电极电解CuCl2溶液为例:总反应方程式:CuCl2=====Cu+Cl2↑。(4)电解池中电子和离子的移动方向①电子:从电源负极流出后,流向电解池阴极;从电解池的阳极流向电源的正极。②离子:阳离子移向电解池的阴极,阴离子移向电解池的阳极。3.电解产物的判断及有关反应式的书写(1)首先判断阴、阳极,分析阳极材料是惰性电极还是活泼电极。(2)再分析电解质水溶液的组成,找全离子并分阴、阳两组(勿忘水溶液中的H+和OH-)。(3)排出阴、阳两极的放电顺序(4)分析电极反应,判断电极产物,写出电极反应式,要注意遵循原子守恒、电荷守恒和电子转移守恒。(5)写出电解总反应式在两极转移电子数目相同的前提下,两极反应相加即可得总反应的化学方程式或离子方程式。4.电解规律(1)电解水型续表(2)电解电解质型(3)放H2生碱型(4)放O2生酸型易错警示电解池中方程式书写四个常见失分点的规避(1)书写电解池中电极反应式时,要以实际放电的离子表示,但书写总电解反应方程式时,弱电解质要写成分子式。(2)阴极不管是什么材料,电极本身都不反应,一定是溶液(或熔融电解质)中的阳离子放电。(3)要确保两极电子转移数目相同,且注明条件“电解”。(4)电解水溶液时,应注意放电顺序中H+、OH-之后的离子一般不参与放电。即不可能用电解水溶液的方法得到K、Ca、Na、Mg、Al等金属。判断正误,正确的画“√”,错误的画“×”。(1)任何化学反应都可以设计成电解池反应。()(2)电解质溶液的导电过程就是电解质溶液被电解的过程。()(3)某些不能自发进行的氧化还原反应,通过电解可以实现。()(4)电解CuCl2溶液,阴极逸出的气体能够使湿润的淀粉碘化钾试纸变蓝色。()(5)电解盐酸、硫酸等溶液,H+放电,溶液的pH逐渐增大。()(6)电解时,电解液中阳离子移向阳极,发生还原反应。()提示(1)×(2)√(3)√(4)×(5)×(6)×题组一电极反应式、电解总反应式的书写1.按要求书写有关的电极反应式及总反应式。(1)以惰性电极电解FeCl2和HCl的混合物可制备FeCl3和H2。阳极反应式:________________________________________;阴极反应式:________________________________________;总反应离子方程式:__________________________________。(2)以铝材为阳极,在H2SO4溶液中电解,铝材表面可形成氧化膜。阳极反应式:________________________________________;阴极反应式:________________________________________;总化学方程式:______________________________________。(3)用惰性电极电解NaCl和CuSO4的混合溶液,电解过程中两极均有两种产物产生,判断阴、阳两极的产物并根据电解的先后顺序写出电极反应方程式。①阳极产物:______________________________________________;电极反应:__________________________________________。②阴极产物:_______________________________________________;电极反应:___________________________________________。答案(1)Fe2+-e-===Fe3+2H++2e-===H2↑2Fe2++2H+=====2Fe3++H2↑(2)2Al-6e-+3H2O===Al2O3...