第2课时元素周期律【目标导航】1
通过分析1~18号元素原子核外电子排布、原子半径、主要化合价的变化,总结出它们的递变规律,并由此认识元素周期律
初步认识元素性质的周期性变化是元素原子核外电子排布周期性变化的必然结果
【自主学习】一、原子结构的周期性变化1.原子序数(1)概念:按__________由小到大的顺序给元素编号,这种编号叫做原子序数
(2)数量关系:原子序数=________=______________=__________
2.原子结构的周期性变化(1)原子最外层电子排布的变化规律随着原子序数的递增,元素原子最外层电子的排布呈现________变化,除____________元素外,最外电子层上的电子数重复出现从____递增到____的变化
(2)元素原子半径的变化规律(稀有气体除外)原子电子层数原子序数原子半径的变化23~9逐渐________311~17逐渐________结论随着原子序数的递增,元素原子半径呈现______变化[议一议]1.解释下列问题:(1)对于电子层数相同的原子,为什么其核电荷数越多,原子半径越小(稀有气体除外)
(2)最外层电子数相同的原子,原子半径的大小与什么因素有关
(3)原子序数越大,原子半径一定越大吗
(4)电子层数相同的元素,原子序数越大,其离子半径越小吗
2.比较下列原子半径的大小:(1)r(Na)________r(S);(2)r(O)________r(S);(3)r(Na)________r(Na+);(4)r(O)________r(O2-)
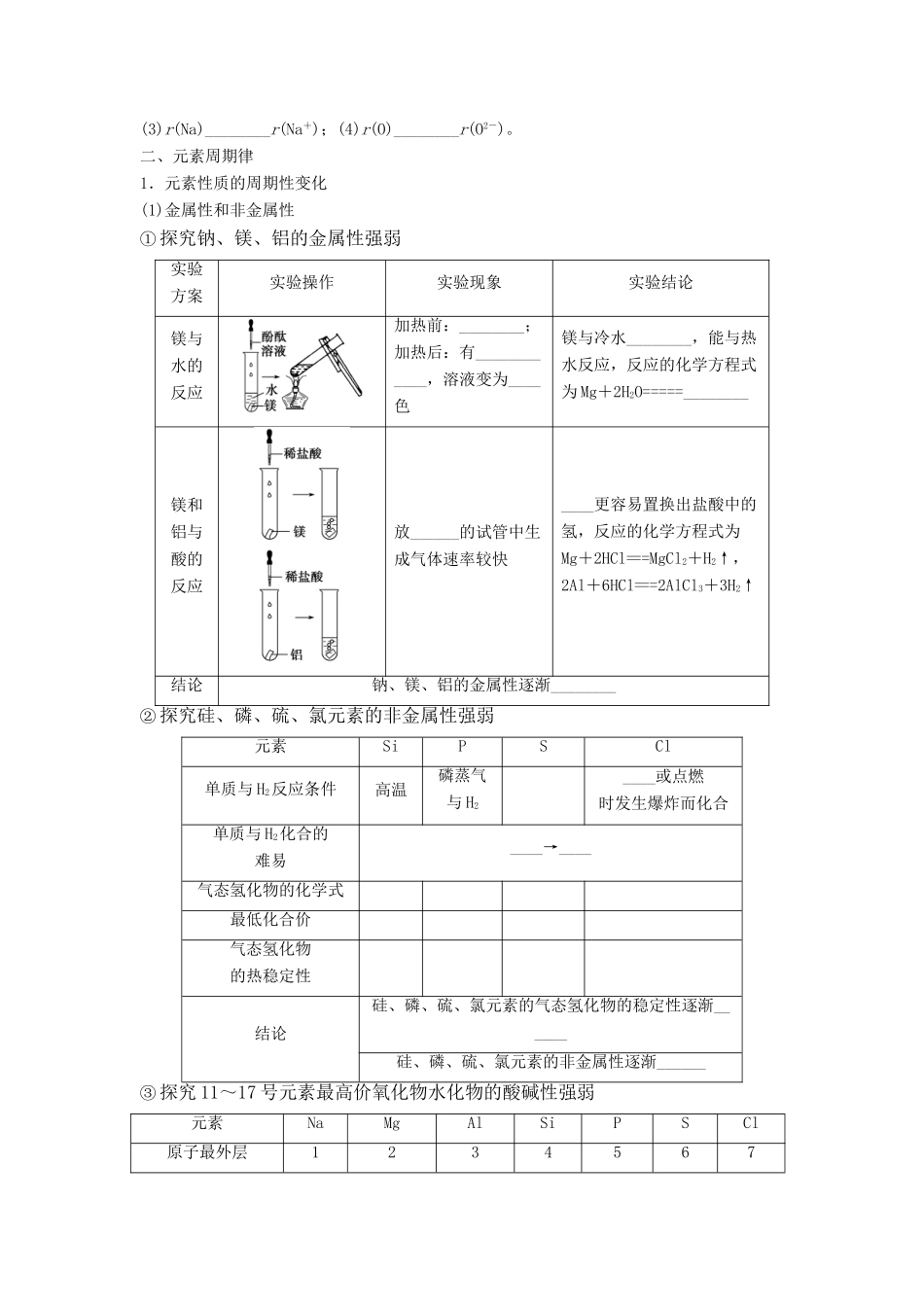
二、元素周期律1.元素性质的周期性变化(1)金属性和非金属性①探究钠、镁、铝的金属性强弱实验方案实验操作实验现象实验结论镁与水的反应加热前:________;加热后:有____________,溶液变为____色镁与冷水________,能与热水反应,反应的化学方程式