江苏省灌南高级中学高二化学:原电池(1)导学案学习目标:1
结合“双液”电池进一步了解原电池的工作原理,完善构成原电池的条件
2.能够写出原电池的电极反应式和总反应式,准确判断电池的正负极、电子及溶液中离子的移动方向
学习过程【自学准备与知识导学】学点1原电池【新课探究】探索新知识:活动与探究一:向一支小烧杯中加入1
0mol/LCuSO4溶液约30ml,再加入适量锌粉,用温度计测量溶液的温度,观察温度计的变化
结论:活动与探究二能否根据Zn+Cu2+=Zn2++Cu也来设计一个铜、锌原电池
指出所选用的电解质溶液,写出该原电池的两电极反应式、总反应式
画出原电池的构造图
负极材料_____负极反应_____________正极材料_____正极反应________________选用的电解质溶液____________原电池的构造图:[问]原电池要构成闭合回路,往往是将两极插入同一池内,那么,原电池的两极是否一定要插入同一池内呢
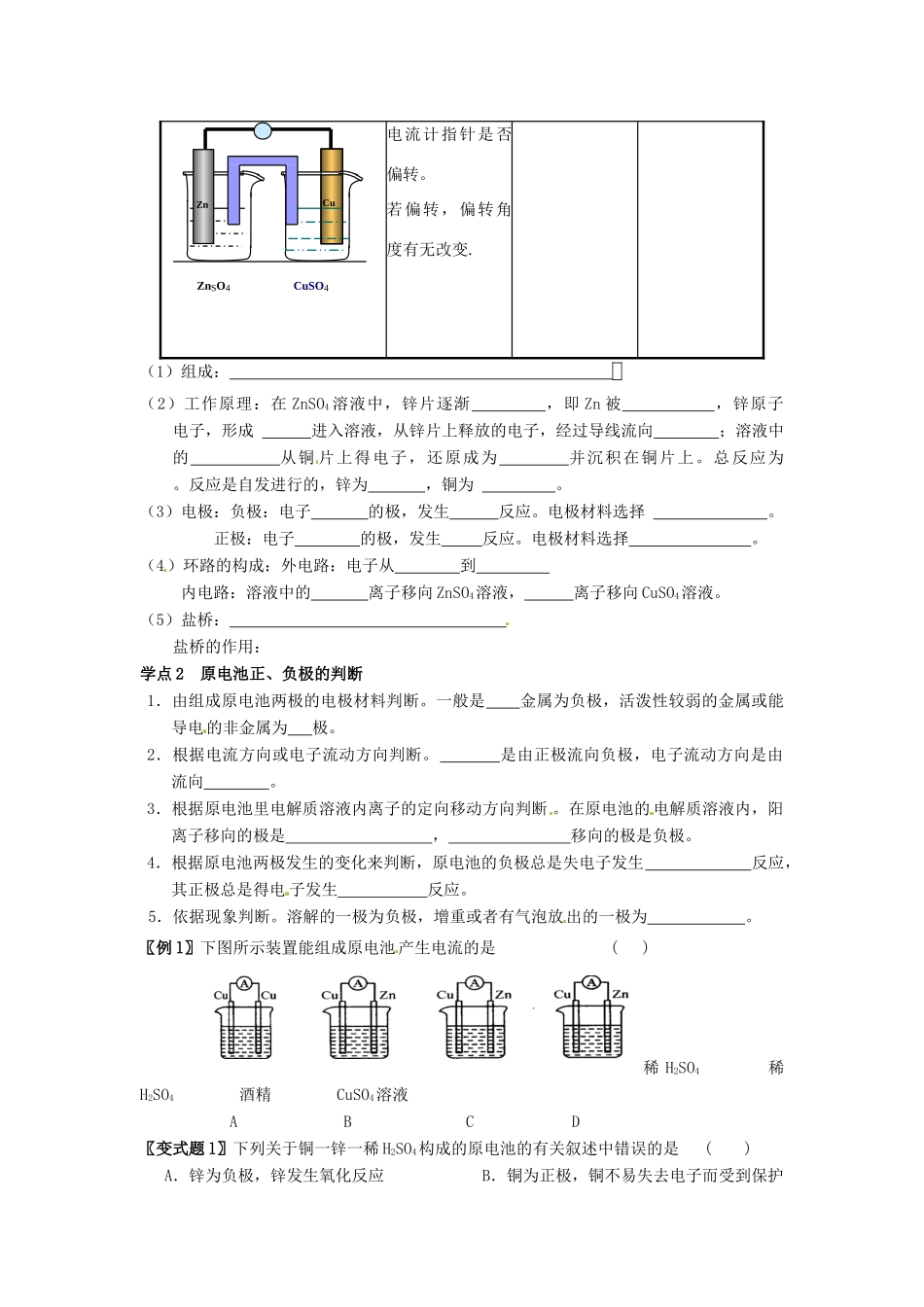
设计图观察记录现象结论电流计指针是否偏转
若偏转,偏转角度有无改变
(1)组成:(2)工作原理:在ZnSO4溶液中,锌片逐渐,即Zn被,锌原子电子,形成进入溶液,从锌片上释放的电子,经过导线流向;溶液中的从铜片上得电子,还原成为并沉积在铜片上
反应是自发进行的,锌为,铜为
(3)电极:负极:电子的极,发生反应
电极材料选择
正极:电子的极,发生反应
电极材料选择
(4)环路的构成:外电路:电子从到内电路:溶液中的离子移向ZnSO4溶液,离子移向CuSO4溶液
(5)盐桥:盐桥的作用:学点2原电池正、负极的判断1.由组成原电池两极的电极材料判断
一般是金属为负极,活泼性较弱的金属或能导电的非金属为极
2.根据电流方向或电子流动方向判断
是由正极流向负极,电子流动方向是由流向
3.根据原电池里电解质溶液内离子的定向移动方向判断