高一年级化学学科学案原子结构、同位素班级_______姓名_________学号_______【学习目标】1.了解原子结构及微粒中质子、电子、中子的计算2.了解元素、核素、同位素的概念【课前检测】1.以下是一些科学家为探索原子结构所作出的重大贡献,请你以连线表示其对应关系
①道尔顿a、提出原子由原子核和电子构成②汤姆生b、发现原子中存在电子③卢瑟福c、提出原子核外电子在一系列稳定的轨道上运动④玻尔d、提出原子学说【新课引入】原子是构成物质的一种微粒,原子是否可以再分,它是由哪些更小的微粒构成呢
相对原子质量定义为“某原子的质量与C-12原子质量的1/12的比”,C-12原子指的是什么
【概念形成】一、原子的构成1.原子的构成:⑴质量关系:⑵电量关系:中性原子:核电荷数质子数核外电子数阴离子:核电荷数质子数核外电子数阳离子:核电荷数质子数核外电子数结合P31表1-7原子质子数(Z)中子数(N)质子数(Z)+中子数(N)相对原子质量F91018
998Na111222
990Al131426
982将有关原子的质子数和中子数之和填表,并与原子的相对原子质量作比较,你能的出什么结论
2.质量数用符号表示
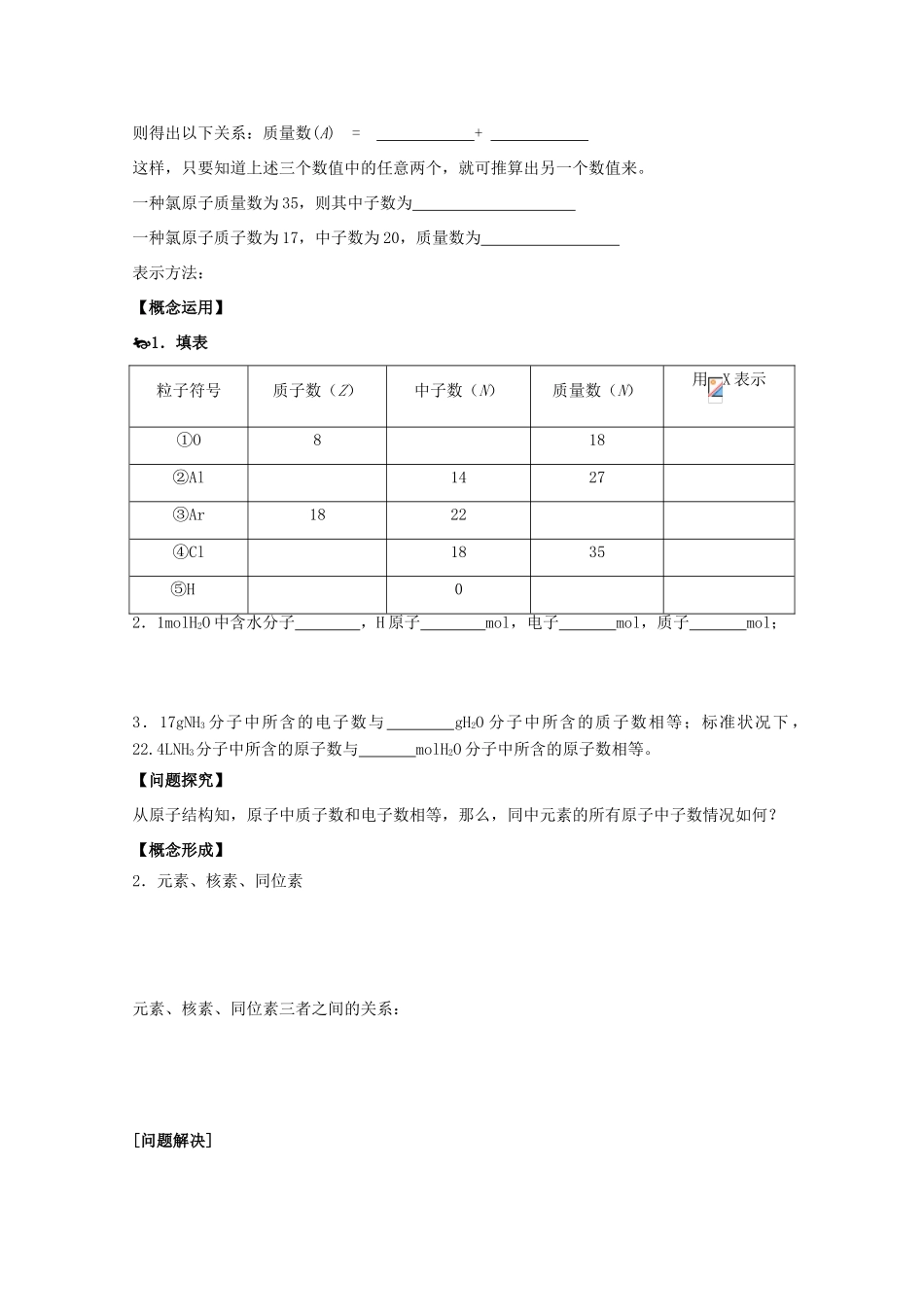
则得出以下关系:质量数(A)=+这样,只要知道上述三个数值中的任意两个,就可推算出另一个数值来
一种氯原子质量数为35,则其中子数为一种氯原子质子数为17,中子数为20,质量数为表示方法:【概念运用】1.填表粒子符号质子数(Z)中子数(N)质量数(N)用X表示①O818②Al1427③Ar1822④Cl1835⑤H02.1molH2O中含水分子,H原子mol,电子mol,质子mol;3.17gNH3分子中所含的电子数与gH2O分子中所含的质子数相等;标准状况下,22
4LNH3分子中所含的原子数与molH2O分子中所含的原子数相等
【问题探究】从原子结构知,原子中质子数和电子数