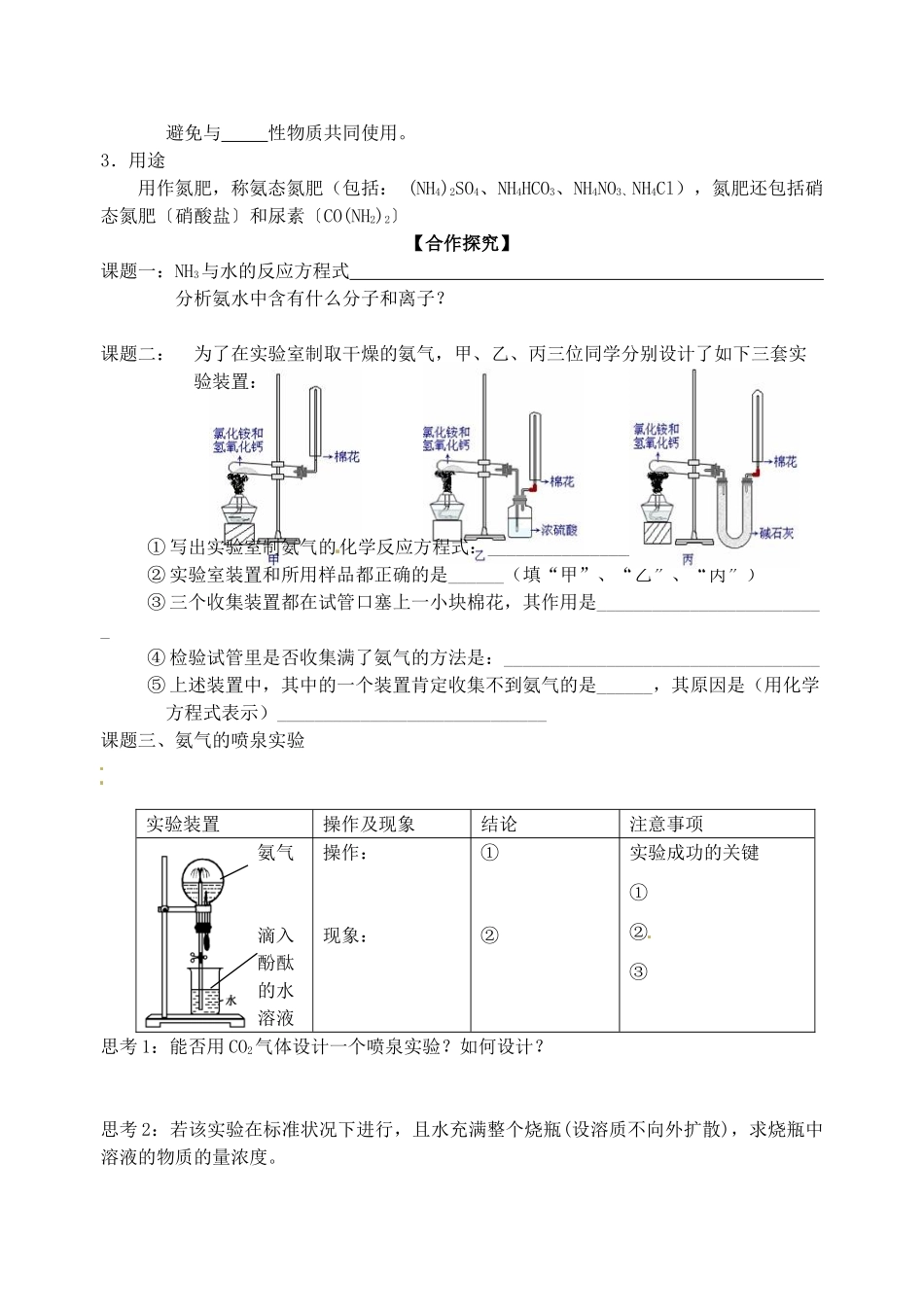
河北省邯郸四中高一化学《422氮肥的生产和使用》导学案【自主学习】一、氨1、物理性质:通常状况下___色_________的气体,密度_____空气,_____溶于水(1:)氨气易_____,液氨汽化时_____大量热,工业上可用作_______
2、化学性质(1)与水的反应:方程式___________________________氨气溶于水形成_______,大部分NH3与水结合成________,NH3·H2O部分电离显弱_______
氨水使红色的石蕊试纸________,氨水的密度______水(填“大于”或“小于”)
NH3·H2O不稳定,受热时易分解(2)与酸反应:能与盐酸、硫酸、硝酸等酸反应
NH3+HCl——(现象:________应用:_____________)NH3+CO2+H2O——或NH3+CO2+H2O——NH3+H2SO4——或NH3+H2SO4——NH3+HNO3——(3)还原性4NH3+5O24NO+6H2O(工业制备硝酸的基础)3、制法(1)实验室制法原理:NH4Cl+Ca(OH)2——装置:_______________;收集:______________;验满:方法一___________、方法二__________
注意:①原料:NH4Cl和Ca(OH)2
②干燥:用(而不用)(2)工业制法N2+H2——二、铵盐1.物理性质:色、溶于水2.化学性质(1)铵盐与碱共热NH4Cl+NaOH――(应用:检验)离子方程式:(2)铵盐受热分解NH4Cl——NH4HCO3——注意:铵盐必须保存在的地方,避免与性物质共同使用
3.用途用作氮肥,称氨态氮肥(包括:(NH4)2SO4、NH4HCO3、NH4NO3、NH4Cl),氮肥还包括硝态氮肥〔硝酸盐〕和尿素〔CO(NH2)2〕【合作探究】课题一:NH3与水的反应方程式分析氨水中含有什么分子和