高一化学化学计算专题复习一:差量法人教版【本讲教育信息】一
教学内容:化学计算专题复习一:差量法化学反应中任何两个量的差与其中任何一个量成正比关系;任何两个量的和与其中任何一个量成正比关系,应用以上关系解题的方法即差量法或和量法
【典型例题】[例1]把氯气通入浓氨水中,发生下列反应,把1
12L氯氮混合气(90%氯气和10%氮气)通过浓氨水,实验测得逸出气体(除氨气和水蒸气)体积为0
672L(50%氯气和50%的氮气)问有多少克氨被氧化
(体积已换算成标准状况)解析:解:设反应中有xg氨被氧化,根据方程式8mol氨有2mol被氧化,解之:[例2]在500mLlmol/L的硫酸铜溶液中,放入一块铁片反应一段时间后,将铁片取出洗净干燥后称量,铁片质量增加了,问析出了多少克铜
反应后硫酸亚铁摩尔浓度是多少
解析:解:设有铜析出,有ymol硫酸亚铁生成,根据反应方程式有:解之mol,硫酸亚铁的摩尔浓度=mol/L
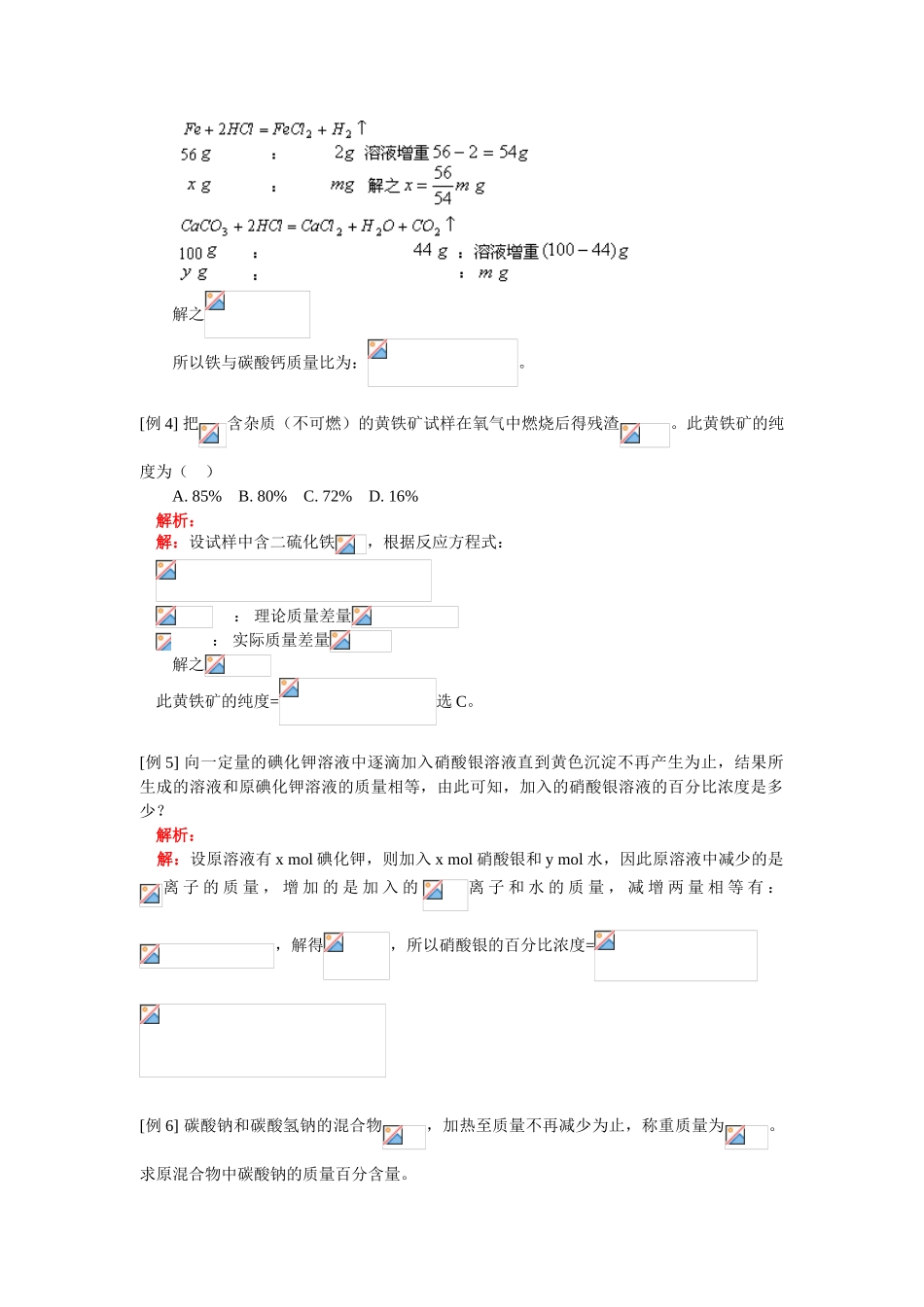
[例3]把盛有等质量盐酸的两个等质量的烧杯,分别置于托盘天平两端,将一定量的铁粉和碳酸钙粉末都溶解后,天平仍保持平衡,则加入的铁粉和碳酸钙粉末的质量比是多少
解析:解:设加入的铁粉和碳酸钙粉末的质量分别为
反应后两烧杯中净增加质量相等,设净增加质量都为,则有:解之所以铁与碳酸钙质量比为:
[例4]把含杂质(不可燃)的黄铁矿试样在氧气中燃烧后得残渣
此黄铁矿的纯度为()A
16%解析:解:设试样中含二硫化铁,根据反应方程式::理论质量差量:实际质量差量解之此黄铁矿的纯度=选C
[例5]向一定量的碘化钾溶液中逐滴加入硝酸银溶液直到黄色沉淀不再产生为止,结果所生成的溶液和原碘化钾溶液的质量相等,由此可知,加入的硝酸银溶液的百分比浓度是多少
解析:解:设原溶液有xmol碘化钾,则加入xmol硝酸银和ymol水,因此原溶液中减少的是离子的质量,增加的