江苏省淮阴中学2009届高三考前热身化学试题答题纸15、Ⅰ、(3分)下列有关实验说法错误的是___________Ⅱ、⑴是溶液中引起的(填微粒的化学式,下同)
是溶液中引起的
假设1方案:
假设2方案:
⑵,你认为(填“假设1”或“假设2”)的推断是正确的;_(填“行”或“否”),理由是:
⑶反应的离子方程式为:
16、(1)C与K的混合物工业上称为____________________________(2)写出电解E水溶液的化学方程式__________________________________________
(3)J与H反应的离子方程式为
则A、B的物质的量之比为_____________
17、(1)流程①中所得MnSO4溶液的pH比软锰矿浆的pH(填“大”或“小”)
(2)反应②的目的是将溶液中的Fe2+氧化成Fe3+,其离子反应方程式为
(3)反应③中硫化钠的作用是使重金属离子转化为硫化物沉淀(不考虑Fe3+与S2-反应),碳酸钙的作用是
(4)加入稍过量的NH4HCO3的目的是,溶液的pH不能过低的原因是
(5)其中工艺A的优点是
(答对1个即可)18、(1)热化学方程式:
电池负极的反应式为
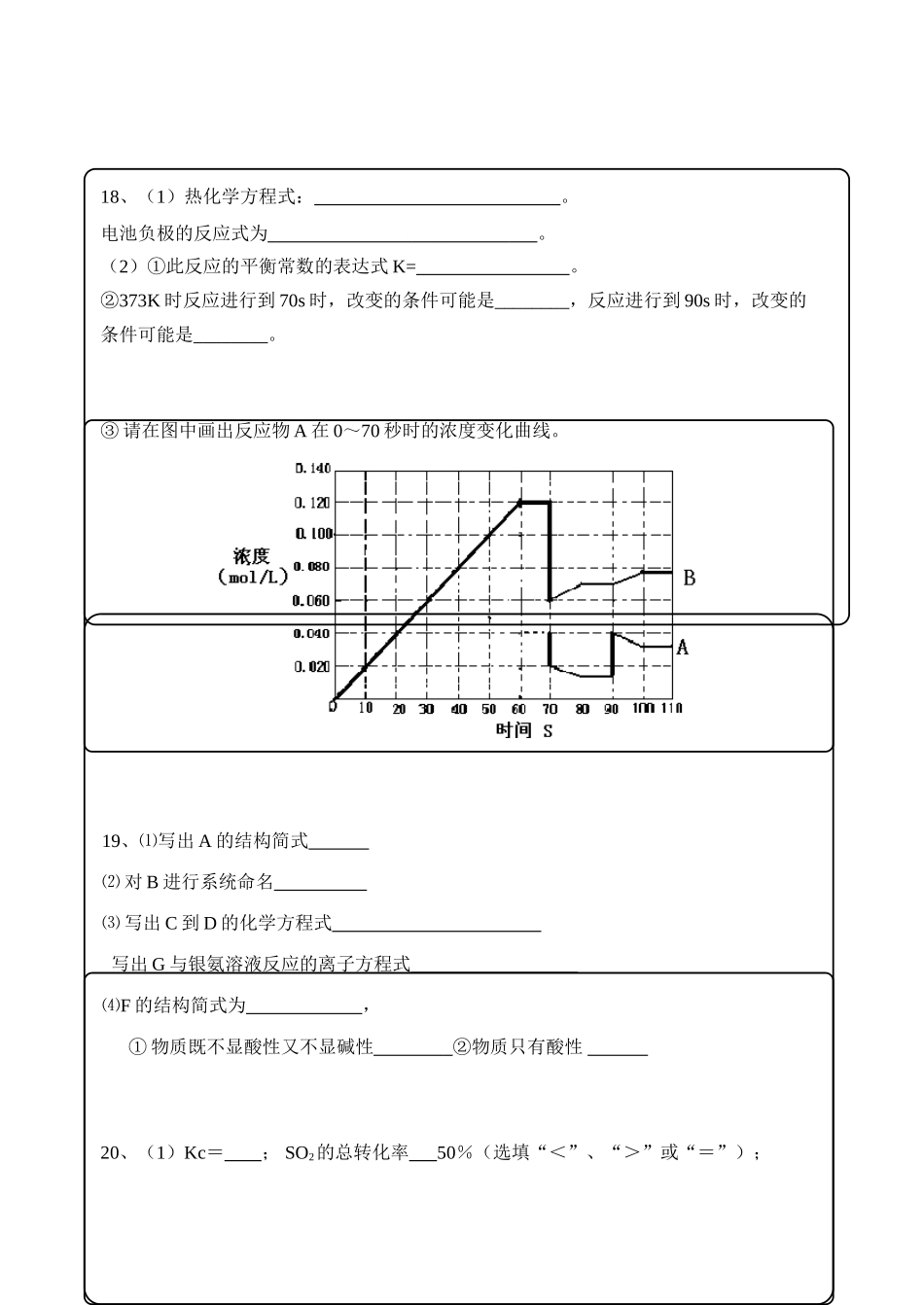
(2)①此反应的平衡常数的表达式K=
②373K时反应进行到70s时,改变的条件可能是________,反应进行到90s时,改变的条件可能是________
③请在图中画出反应物A在0~70秒时的浓度变化曲线
19、⑴写出A的结构简式⑵对B进行系统命名⑶写出C到D的化学方程式写出G与银氨溶液反应的离子方程式⑷F的结构简式为,①物质既不显酸性又不显碱性②物质只有酸性20、(1)Kc=;SO2的总转化率50%(选填“<”、“>”或“=”);(2)写出总反应方程式,
(3)则x=,体积V=L
21、(1)元素“O”原子结构示意图是
(2)画出“c”的电子排布式