第2节原电池化学电源1.了解原电池的工作原理,能写出电极反应和电池反应方程式
2.了解常见化学电源的种类及其工作原理
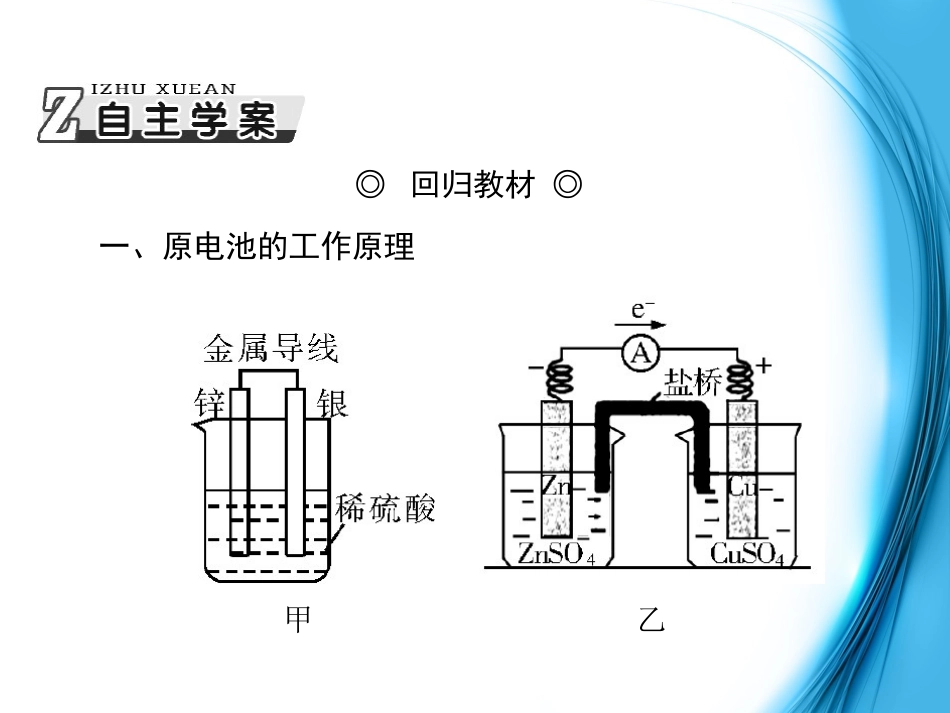
◎回归教材◎一、原电池的工作原理甲乙项目内容定义将________________________的装置称为原电池能量转化化学能转化为电能(提供电流)形成条件自发的氧化还原反应具有__________________做电极具有电解质溶液具有(导线相连组成)闭合回路电极判断负极(较活泼的金属)——________电子——发生________正极(较不活泼的金属或非金属)——________电子——发生________化学能转化为电能活动性不同的金属失氧化反应得还原反应(续表)项目内容电极反应式(如图甲)负极:__________________________正极:__________________________总反应:Zn+2H+===Zn2++H2↑微粒移动方向电子流向:__________→→导线__________电流流向:__________→→导线__________离子流向:阳离子移向__________,阴离子移向__________盐桥的作用阻止反应物的________;盐桥中离子的定向迁移构成了电流通路,既构成了________,又使溶液保持________,反应可以继续进行Zn-2e-===Zn2+2H++2e-===H2↑负极正极正极负极正极负极直接接触闭合回路电中性二、化学电源1.一次电池:不能充电,不能反复使用
化学电源碱性锌锰电池锌银电池正极反应式2MnO2+2H2O+2e-===2MnOOH+2OH-Ag2O+H2O+2e-===2Ag+2OH-负极反应式____________________________________Zn+2OH-—2e-===Zn(OH)2总反应方程式Zn+2MnO2+2H2O===2MnOOH+