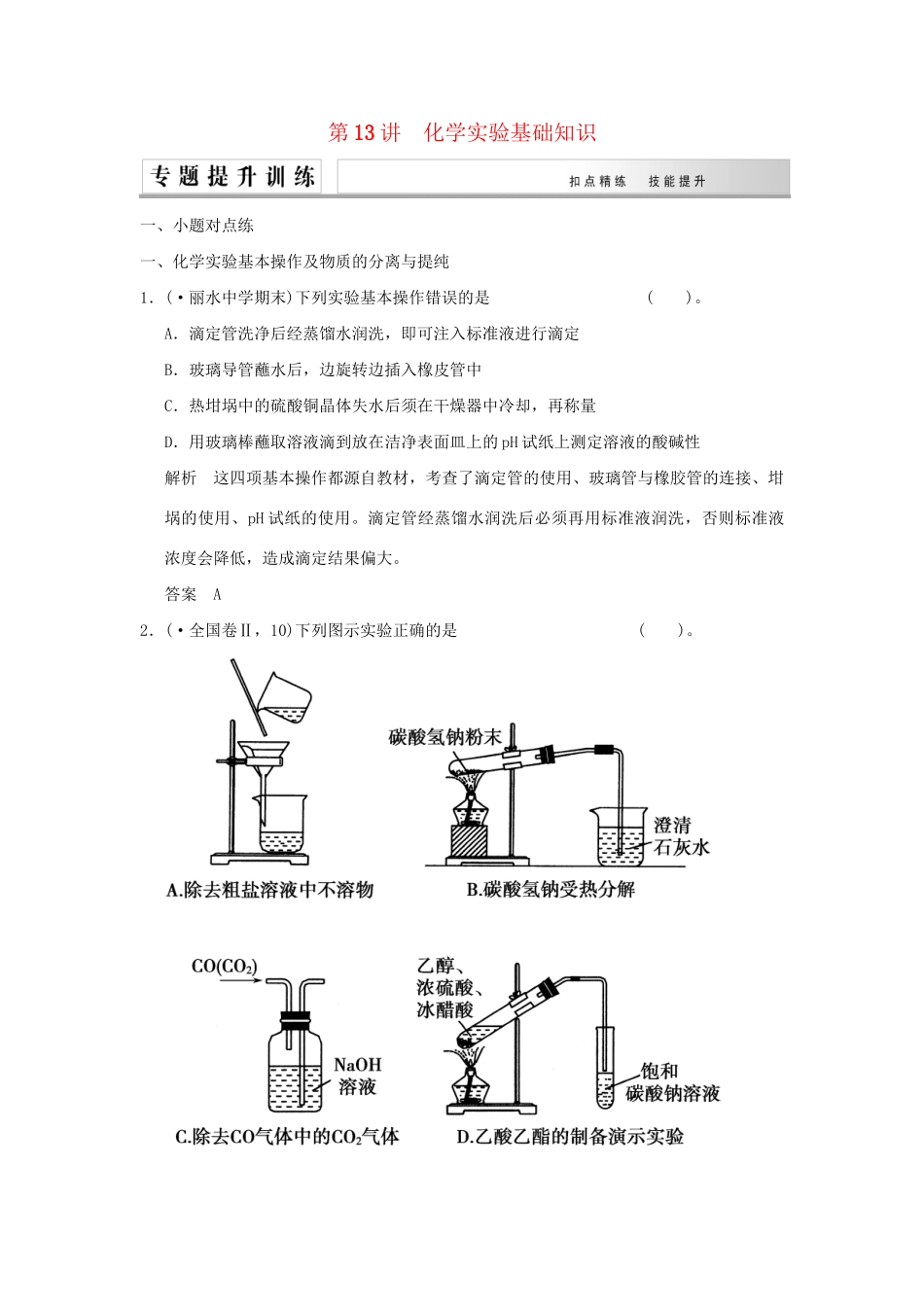
第13讲化学实验基础知识一、小题对点练一、化学实验基本操作及物质的分离与提纯1.(·丽水中学期末)下列实验基本操作错误的是()。A.滴定管洗净后经蒸馏水润洗,即可注入标准液进行滴定B.玻璃导管蘸水后,边旋转边插入橡皮管中C.热坩埚中的硫酸铜晶体失水后须在干燥器中冷却,再称量D.用玻璃棒蘸取溶液滴到放在洁净表面皿上的pH试纸上测定溶液的酸碱性解析这四项基本操作都源自教材,考查了滴定管的使用、玻璃管与橡胶管的连接、坩埚的使用、pH试纸的使用。滴定管经蒸馏水润洗后必须再用标准液润洗,否则标准液浓度会降低,造成滴定结果偏大。答案A2.(·全国卷Ⅱ,10)下列图示实验正确的是()。解析A项,“”过滤时要求一贴、二低、三靠,该实验中玻璃棒悬在漏斗上方,没有靠在三层滤纸上,且漏斗颈尖嘴一侧应紧贴烧杯内壁,错误;B项,加热分解碳酸氢钠时,因为有水生成,试管口应稍向下倾斜,错误;C项,混合气体应长进短出,错误。答案D3.下列说法正确的是()。A.久置的浓HNO3呈黄色,为除去黄色可通入O2B.NH4Cl固体中混有I2,可用加热的方法除去C.为除去FeSO4溶液中的Fe2(SO4)3,可加入Cu粉D.为除去CO2中少量的SO2,可使其通过澄清石灰水解析该题主要考查了用化学方法分离、提纯物质的方法。久置的浓HNO3呈黄色是由于硝酸分解生成的NO2溶解导致,通入O2发生反应:4NO2+O2+2H2O===4HNO3,从而可以除去黄色,A正确;NH4Cl固体中混有I2,加热时,I2升华,NH4Cl也分解为NH3和HCl,B错误;FeSO4溶液中混有Fe2(SO4)3,加入Cu粉,发生反应:Fe2(SO4)3+Cu===2FeSO4+CuSO4,虽然除去了Fe2(SO4)3,但引入了新杂质CuSO4,C错误;SO2、CO2均能与澄清石灰水反应,除去CO2中少量的SO2,应使其通过饱和NaHCO3溶液:NaHCO3+SO2===NaHSO3+CO2,D错误。答案A二、物质的检验4.(·重庆理综,2)下列实验可实现鉴别目的的是()。A.用KOH溶液鉴别SO3(g)和SO2B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2C.用CO2鉴别NaAlO2溶液和CH3COONa溶液D.用BaCl2溶液鉴别AgNO3溶液和K2SO4溶液解析A项,SO3(g)和SO2均能与KOH反应且没有明显的现象;B项,Br2(g)和NO2均具有氧化性,均能使湿润碘化钾淀粉试纸变蓝;C项,CO2与NaAlO2溶液反应生成白色沉淀Al(OH)3,CO2与CH3COONa不反应;D项,AgNO3溶液和K2SO4溶液与BaCl2溶液反应均生成白色沉淀,错误。答案C5.(·浙江名校联盟二联)某钠盐溶液中可能含有NO、SO、SO、CO、Cl-、I-等阴离子。某同学取5份此溶液样品,分别进行了如下实验:①用pH计测得溶液的pH大于7②加入盐酸,产生有色、有刺激性气味气体③加入硝酸酸化的AgNO3溶液,产生白色沉淀,且放出有色、有刺激性气味气体④加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色⑤加入足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色该同学最终确定该钠盐溶液中仅含NO、CO、Cl-三种阴离子。请分析,该同学只需要完成上述哪几个实验,即可得出结论()。A.①②④⑤B.③④C.③④⑤D.②③⑤解析由①溶液的pH大于7,溶液呈碱性,知此溶液中至少有一种弱酸根离子;②加入盐酸,产生有色、有刺激性气味气体,可推知原溶液中有NO;③加入硝酸酸化的AgNO3溶液,产生白色沉淀,且放出有色、有刺激性气味气体,可确定原溶液中有Cl-、NO,无I-;④加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色,确定有CO,无SO,综合③和④即可得到实验结论。答案B三、气体制备实验中仪器的组装与创新6.(·北京理综,11)用下图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是()。①中实验②中现象A铁粉与水蒸气加热肥皂水冒泡B加热NH4Cl和Ca(OH)2混合物酚酞溶液变红CNaHCO3固体受热分解澄清石灰水变浑浊D石蜡油在碎瓷片上受热分解Br2的CCl4溶液褪色解析A项,Fe与水蒸气高温反应产生H2,但加热时,反应装置中空气受热膨胀,以及水蒸气均会使②中肥皂水冒泡,错误;B项NH4Cl和Ca(OH)2加热产生NH3,NH3溶于水生成NH3·H2O,NH3·H2ONH+OH-,使酚...