选修四第三章第三节电解池(第二课时)一、电解:电流通过电解质溶液(或熔融电解质)而在阴、阳两极引起氧化还原反应的过程
理解:电解质溶液导电的过程就是过程
电解电解是非自发地将能转化为能
电化学1、电解池(槽):电能转化为化学能的装置
2、构成电解池的条件:(1)直流电源(2)两个电极;(3)电解质溶液或熔融的电解质;(4)闭合回路
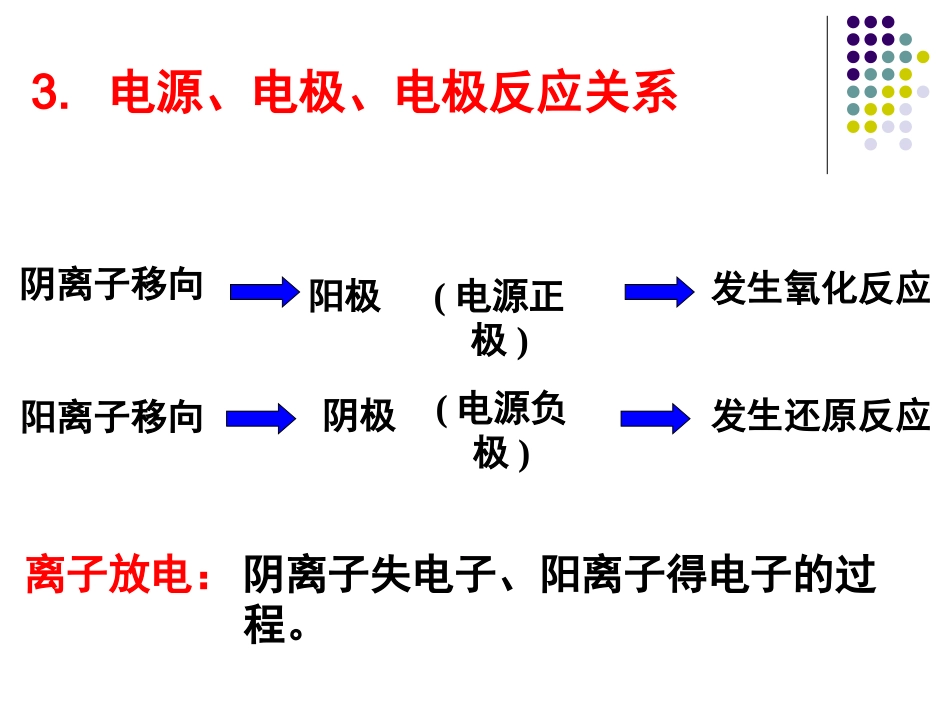
(复习回顾)发生氧化反应阴离子移向阳极(电源正极)3
电源、电极、电极反应关系阴极(电源负极)发生还原反应阳离子移向离子放电:阴离子失电子、阳离子得电子的过程
4、离子放电顺序:1、阳离子放电(得电子)顺序:Ag+>Hg2+>Fe3+>Cu2+>H+(水)>Pb2+>Sn2+>Fe2+>Zn2+>Al3+>Mg2+>Na+>Ca2+>K+2、阴离子放电(失电子)顺序:氧化性还原性金属>S2–>I–>Br–>Cl–>OH–(水)>含氧酸根(NO3-、SO42–等)>F-注意:若阳极是活性电极(石墨、金、铂之外)阳极本身失去电子被氧化,阴离子不在阳极放电;若阳极是惰性电极,还原性强的阴离子在阳极放电,阴极材料不发生任何变化
除Pt、Au①活性材料作电极时:金属在阳极失电子被氧化成阳离子进人溶液,阴离子在电极上不放电
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴离子按顺序放电无论是惰性电极还是活性电极都不参与电极反应,发生反应的是溶液中的阳离子
阳极反应(氧化反应):与电极材料有关阴极反应(还原反应):与电极材料无关总结:总结:分析电解反应的一般思路:明确溶液中存在哪些离子根据阳极氧化、阴极还原分析得出产物判断阳极材料及阴阳两极附近离子种类及离子放电顺序先电离后电解165
电极反应式的书写1
写出用石墨电极电解硫酸铜溶液的电极反应式及总离子反应式2
写出用铜做电极电解硫酸铜溶液的电极反应式阳极4OH--4e-=2H2O+O2↑阴极2Cu2++4e