高一化学化学计量在实验中的应用练习(2)1.填表:物理量摩尔质量符号n单位个gLmol/LNA=_________________________;当M以g/mol为单位时,其数值上等于____________________________________在标准状况下,Vm=__________________________2.完成下列物理量的转换关信息:3.计算下列物质的摩尔质量(1)HNO3___________________________(2)HCl___________________________(3)CH3COOH__________________(4)Na2SO4·10H2O___________________________4.计算下列物质的物质的量1
050×10①23个HCl分子31
8gNa②2CO35
6LCO③2(标准状况下)100mL0
5mol/L④蔗糖溶液中溶质的物质的量5.1
5molH2SO4的质量是______________,其中含有______molO,含有______molH
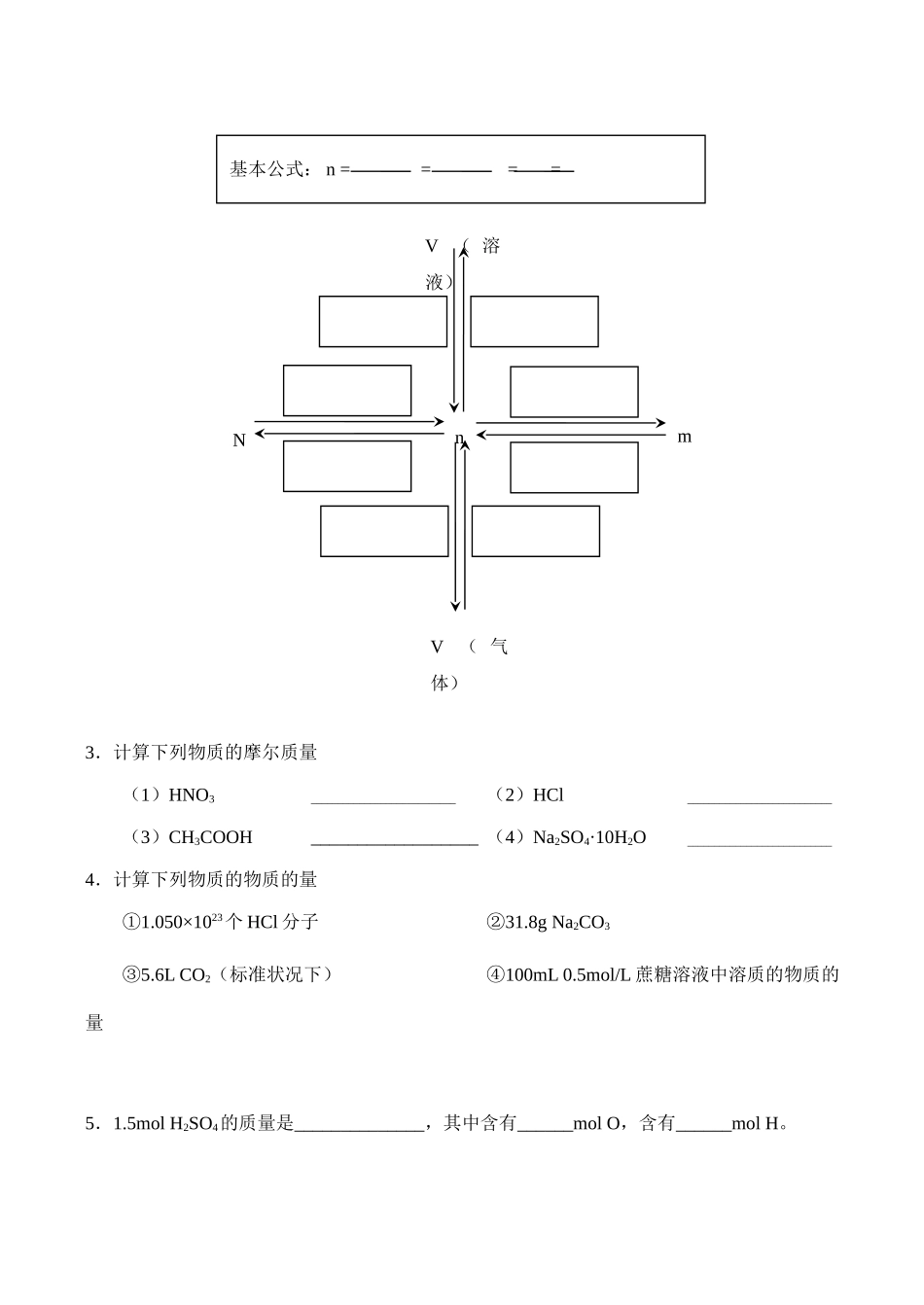
nNmV(气体)V(溶液)基本公式:n====6.在同温同压下,质量相同的①N2、②CO2、③Cl2、④CH4、⑤O2等五种气体所占的体积由大到小的顺序排列为_________________________
7.4gH2与22
4L(标准状况下)CO2相比,所含分子数目多的是__________
01mol某气体的质量为0
44g,该气体的摩尔质量为________________;在标准状况下,该气体的密度为_____________g/L
9.已知在3
2g某气体中所含的分子数目约为3
01×1022,则此气体的相对分子质量为_______
10.在标准状况下,100mL某气体的质量为0
179g,则该气体的相对分子质量为____