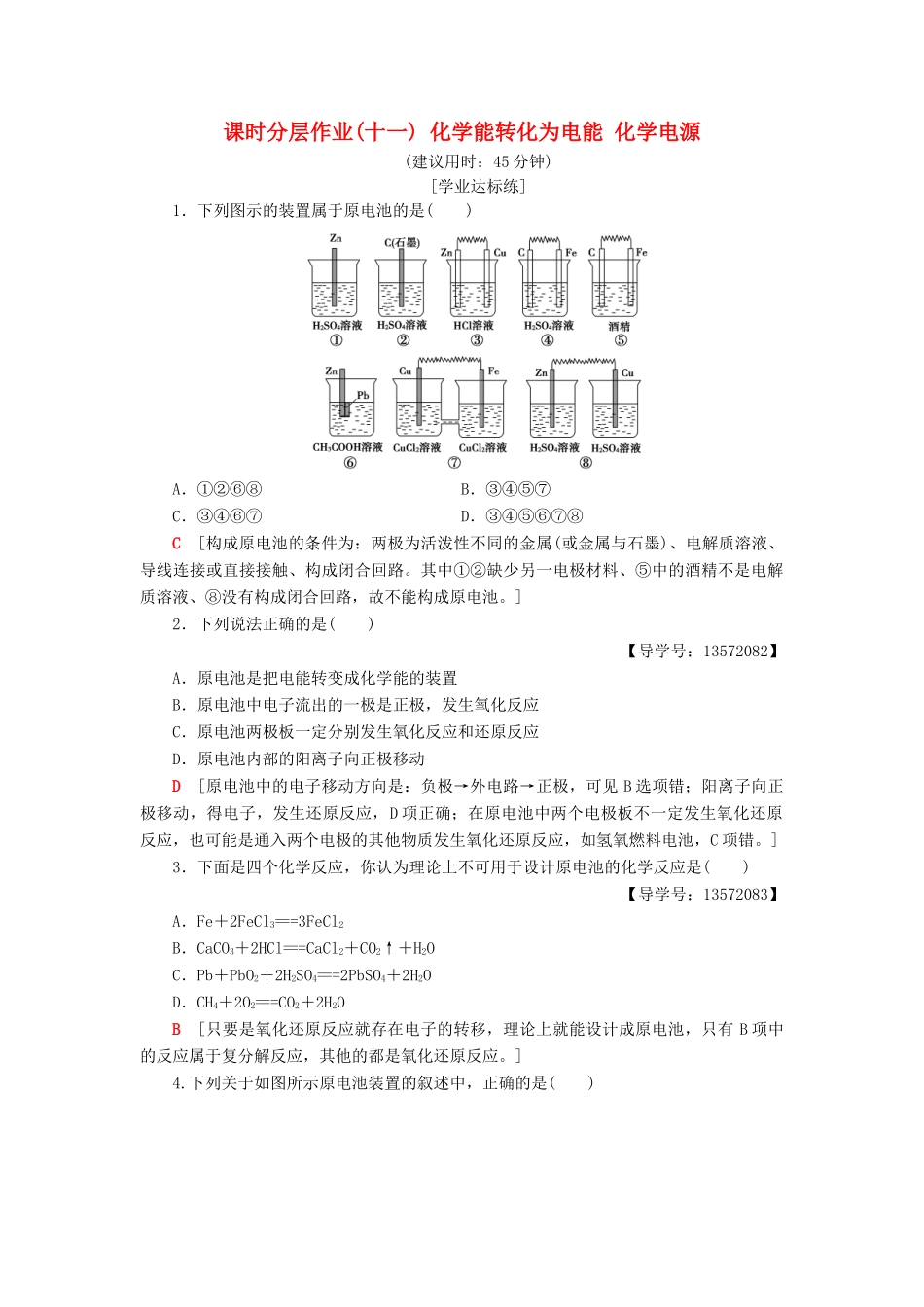
课时分层作业(十一)化学能转化为电能化学电源(建议用时:45分钟)[学业达标练]1.下列图示的装置属于原电池的是()A.①②⑥⑧B.③④⑤⑦C.③④⑥⑦D.③④⑤⑥⑦⑧C[构成原电池的条件为:两极为活泼性不同的金属(或金属与石墨)、电解质溶液、导线连接或直接接触、构成闭合回路
其中①②缺少另一电极材料、⑤中的酒精不是电解质溶液、⑧没有构成闭合回路,故不能构成原电池
]2.下列说法正确的是()【导学号:13572082】A.原电池是把电能转变成化学能的装置B.原电池中电子流出的一极是正极,发生氧化反应C.原电池两极板一定分别发生氧化反应和还原反应D.原电池内部的阳离子向正极移动D[原电池中的电子移动方向是:负极→外电路→正极,可见B选项错;阳离子向正极移动,得电子,发生还原反应,D项正确;在原电池中两个电极板不一定发生氧化还原反应,也可能是通入两个电极的其他物质发生氧化还原反应,如氢氧燃料电池,C项错
]3.下面是四个化学反应,你认为理论上不可用于设计原电池的化学反应是()【导学号:13572083】A.Fe+2FeCl3===3FeCl2B.CaCO3+2HCl===CaCl2+CO2↑+H2OC.Pb+PbO2+2H2SO4===2PbSO4+2H2OD.CH4+2O2===CO2+2H2OB[只要是氧化还原反应就存在电子的转移,理论上就能设计成原电池,只有B项中的反应属于复分解反应,其他的都是氧化还原反应
下列关于如图所示原电池装置的叙述中,正确的是()A.铜片是负极B.氢离子在铜片表面被还原C.电流从锌片经导线流向铜片D.铜片质量逐渐减小B[较活泼的金属锌作负极,较不活泼的金属铜作正极,故A错误;铜是正极,正极上氢离子得电子,发生还原反应生成氢气,所以氢离子在铜片表面被还原,故B正确;电子从负极沿导线流向正极,电流从正极(Cu)流向负极(Zn),故C错误;锌失电