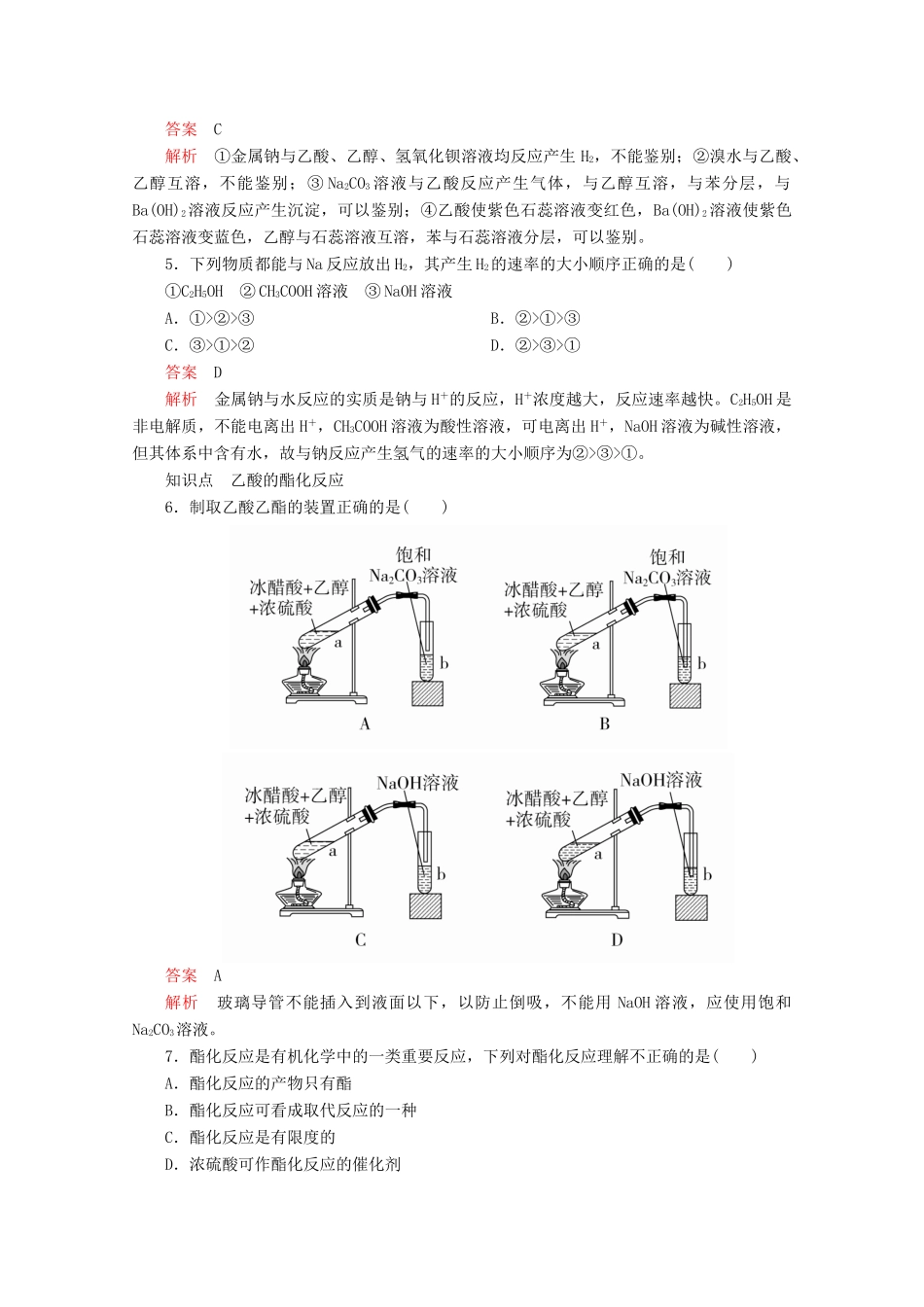
乙酸[A篇知识对点训练]知识点认识乙酸的酸性1.下图所示是某有机物分子的球棍模型,该有机物中含有C、H、O三种元素,下列关于该有机物说法中不正确的是()A.是食醋的主要成分B.其官能团是羧基C.能使酸性KMnO4溶液褪色D.能与碱发生中和反应答案C解析由有机物的球棍模型可知该有机物是CH3COOH
因为CH3COOH分子中的羧基能电离出H+,故能与碱电离产生的OH-发生中和反应
而CH3COOH不能被酸性KMnO4溶液氧化
2.下列事实不能体现乙酸酸性的是()A.乙酸滴入碳酸钠溶液中会出现气泡B.乙酸中滴加几滴石蕊溶液呈红色C.乙酸和水能以任意比例互溶D.长时间使用的热水瓶胆可以用乙酸来洗去水垢答案C解析乙酸与碳酸钠反应的方程式为2CH3COOH+Na2CO3―→2CH3COONa+CO2↑+H2O,体现了乙酸的酸性,A项正确;与指示剂作用是酸的通性之一,B项正确;乙酸和水能以任意比例互溶体现的是乙酸的物理性质,不能体现其酸性,C项错误;水垢的主要成分为CaCO3,乙酸能溶解水垢,体现了乙酸的酸性,D项正确
3.可以说明CH3COOH是弱酸的事实是()A.CH3COOH与水能以任意比混溶B.CH3COOH能与Na2CO3溶液反应,产生CO2气体C.1mol·L-1的CH3COOH溶液的c(H+)比1mol·L-1的盐酸溶液的c(H+)小D.1mol·L-1的CH3COOH水溶液能使紫色石蕊试液变红答案C解析A项CH3COOH与水互溶与酸性强弱无关;B项只能说明CH3COOH酸性强于H2CO3酸性,但无法确定为弱酸;C项能说明CH3COOH发生不完全电离,属于弱酸;D项说明CH3COOH具有酸的通性,能使紫色石蕊试液变红
4.下列物质中,可一次性鉴别乙酸、乙醇、苯及氢氧化钡溶液的是()①金属钠②溴水③碳酸钠溶液④紫色石蕊溶液A.①②B.②③C.③④D.②④答案C解析①金属钠与