南师大第二附属高级中学高三化学二卷典型题训练七1、铁是人体必须的微量元素,治疗缺铁性贫血的常见方法是服用补铁药物
“速力菲”(主要成分:琥珀酸亚铁,呈暗黄色)是市场上一种常见的补铁药物
该药品不溶于水但能溶于人体中的胃酸
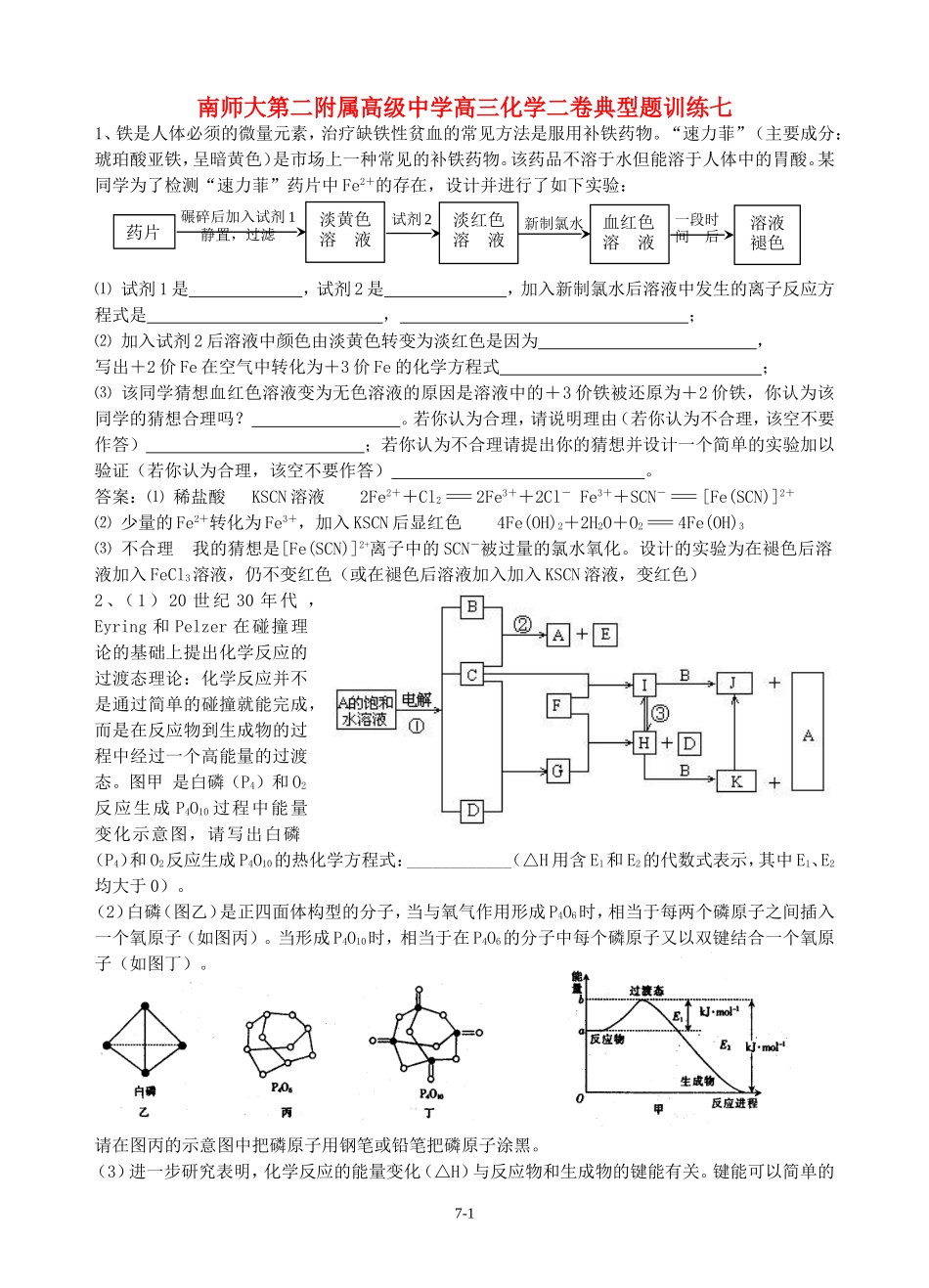
某同学为了检测“速力菲”药片中Fe2+的存在,设计并进行了如下实验:⑴试剂1是,试剂2是,加入新制氯水后溶液中发生的离子反应方程式是,;⑵加入试剂2后溶液中颜色由淡黄色转变为淡红色是因为,写出+2价Fe在空气中转化为+3价Fe的化学方程式;⑶该同学猜想血红色溶液变为无色溶液的原因是溶液中的+3价铁被还原为+2价铁,你认为该同学的猜想合理吗
若你认为合理,请说明理由(若你认为不合理,该空不要作答);若你认为不合理请提出你的猜想并设计一个简单的实验加以验证(若你认为合理,该空不要作答)
答案:⑴稀盐酸KSCN溶液2Fe2++Cl2=2Fe3++2Cl-Fe3++SCN-=[Fe(SCN)]2+⑵少量的Fe2+转化为Fe3+,加入KSCN后显红色4Fe(OH)2+2H2O+O2=4Fe(OH)3⑶不合理我的猜想是[Fe(SCN)]2+离子中的SCN-被过量的氯水氧化
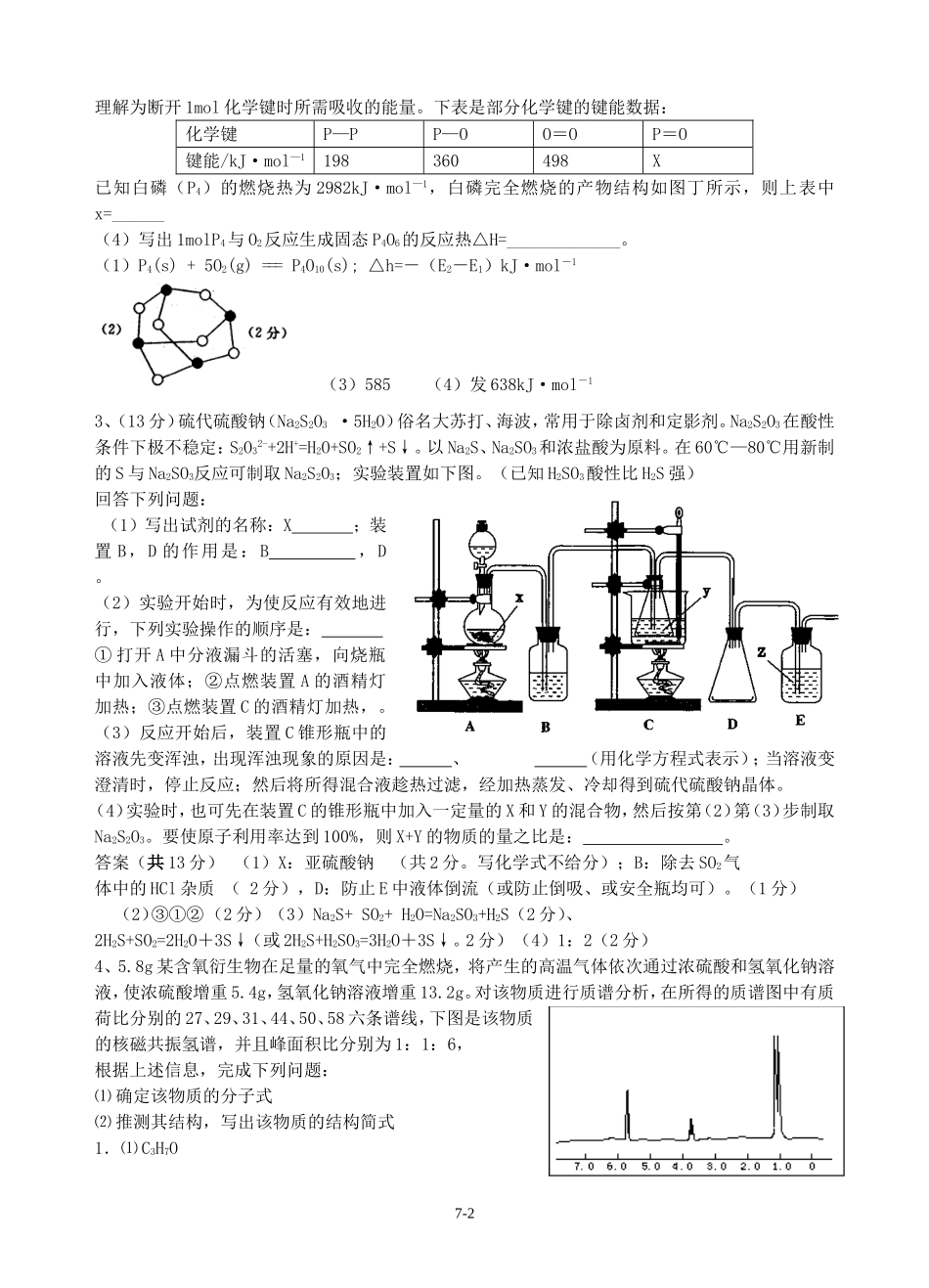
设计的实验为在褪色后溶液加入FeCl3溶液,仍不变红色(或在褪色后溶液加入加入KSCN溶液,变红色)2、(1)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成,而是在反应物到生成物的过程中经过一个高能量的过渡态
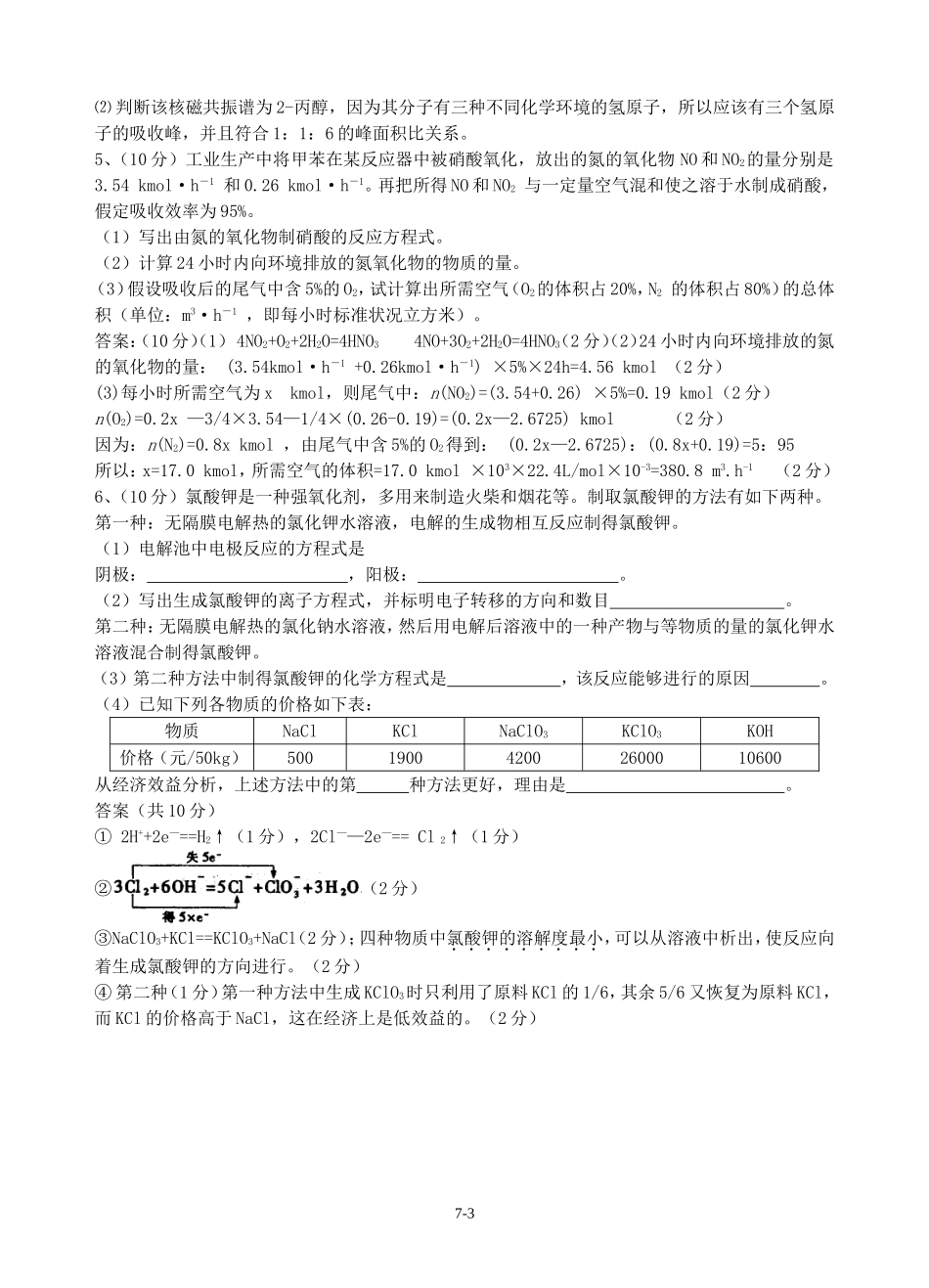
图甲是白磷(P4)和O2反应生成P4O10过程中能量变化示意图,请写出白磷(P4)和O2反应生成P4O10的热化学方程式:____________(△H用含E1和E2的代数式表示,其中E1、E2均大于0)
(2)白磷(图乙)是正四面体构型的分子,当与氧气作用形成P4O6时,相当于每两个磷原子之间插入一个氧原子(如图