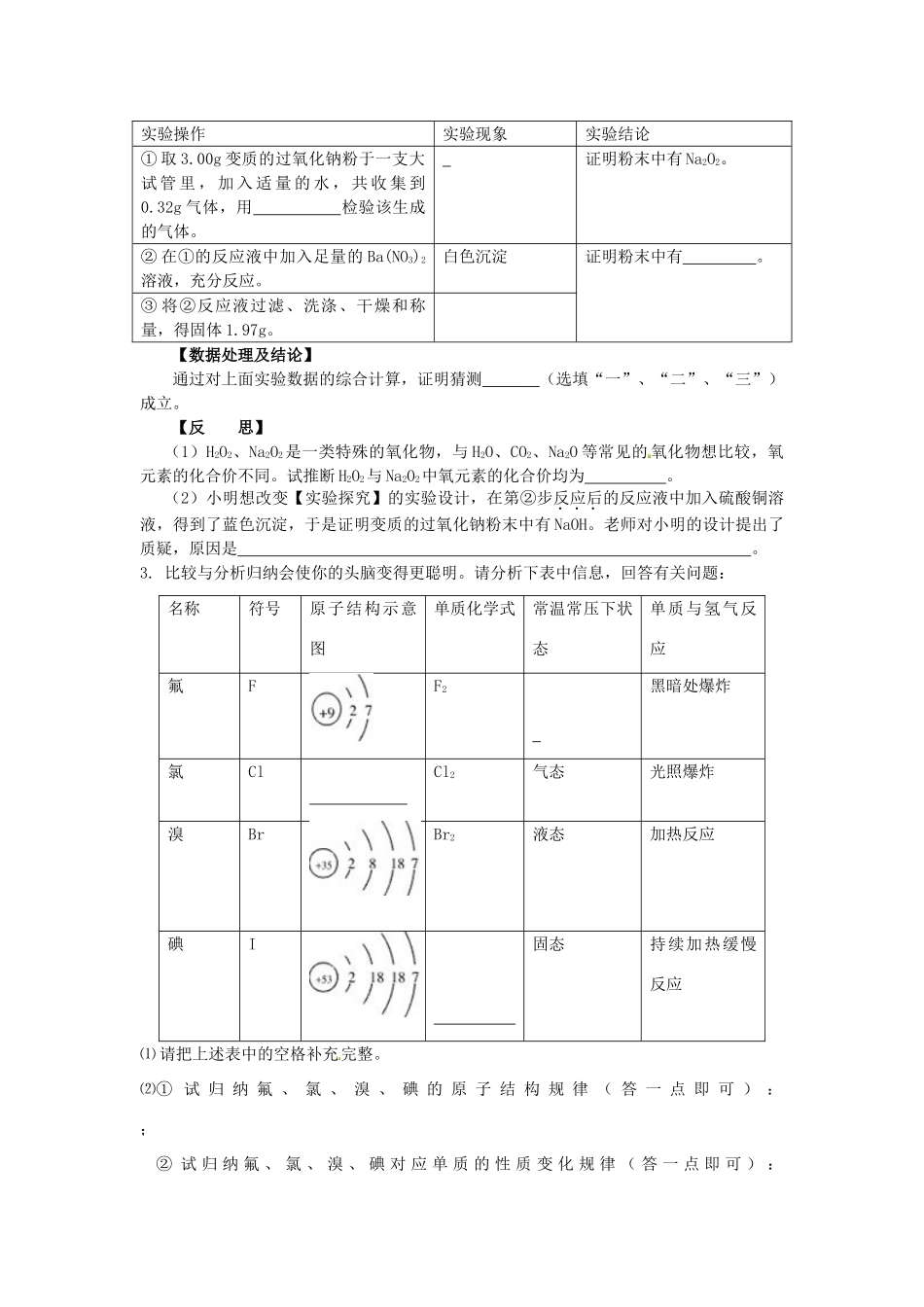
浓硫酸加热O2加热稀硫酸专题复习八:高中化学与初中化学知识衔接信息在中考中的考查1.某校化学兴趣小组的同学在探究金属的化学性质时,发现铜与稀硫酸在常温或加热的条件下均不反应。那么,铜与浓硫酸能否发生反应呢?他们设计了如下图所示装置进行探究。[猜想与假设]①在常温下能反应②常温下不能反应,但在加热条件下能反应③在加热条件下不能反应[查阅资料]含有Cu2+的水溶液通常显蓝色[实验与事实]操作①将一小块铜片放入试管中,加入足量浓硫酸,无明显现象;操作②加热该试管,铜片上有气泡,产生了有刺激性气味的气体;操作③停止加热,将试管中的残液慢慢倒入水中,溶液呈蓝色。[分析与思考]⑴甲同学认为,由以上探究可知:猜想(填序号)是正确的。⑵乙同学认为,经检验产生的气体是SO2,所以铜跟浓硫酸在加热条件下反应的产物只是SO2和CuSO4。⑶丙同学认为,在实验装置中,“蘸有浓碱液棉花”的作用是。[反思与评价]⑷操作③中,从安全角度考虑(填“可以”或“不可以”)将水倒入残液中,其理由是。⑸在[分析与思考]⑵中对产物只是SO2和CuSO4的判断是否准确(填“是”或“否”),其理由是。[拓展与应用]⑹根据以上探究和已掌握的知识,该兴趣小组的同学设计了两个用铜制取硫酸铜的实验方墙案:①CuCuSO4②CuCuOCuSO4经过对两种方案的讨论、对比,同学们认为方案②具有的优点有(填序号),所以工业上制备硫酸铜不是直接利用浓硫酸与铜反应。A.提高铜的利用率B.提高硫酸的利用率C.不产生污染大气的SO2D.不用浓硫酸,安全性好2.“过氧化钠(Na2O2)”是一种淡黄色固体,能与水或二氧化碳反应放出氧气。实验室有一份放置了较长时间的过氧化钠粉末,已发生了部分变质,小明想知道当中的成分,决定开展科学探究。【提出问题】变质的过氧化钠粉末中有哪些成分?【收集资料】2Na2O2+2H2O==4NaOH+O2,2Na2O2+2CO2==2Na2CO3+O2。【猜想】猜测一:变质的过氧化钠粉末是Na2O2和NaOH的混合物;猜测二:变质的过氧化钠粉末是的混合物;猜测三:变质的过氧化钠粉末是Na2O2、NaOH和Na2CO3的混合物。【实验探究】实验操作实验现象实验结论①取3.00g变质的过氧化钠粉于一支大试管里,加入适量的水,共收集到0.32g气体,用检验该生成的气体。证明粉末中有Na2O2。②在①的反应液中加入足量的Ba(NO3)2溶液,充分反应。白色沉淀证明粉末中有。③将②反应液过滤、洗涤、干燥和称量,得固体1.97g。【数据处理及结论】通过对上面实验数据的综合计算,证明猜测(选填“一”、“二”、“三”)成立。【反思】(1)H2O2、Na2O2是一类特殊的氧化物,与H2O、CO2、Na2O等常见的氧化物想比较,氧元素的化合价不同。试推断H2O2与Na2O2中氧元素的化合价均为。(2)小明想改变【实验探究】的实验设计,在第②步反应后的反应液中加入硫酸铜溶液,得到了蓝色沉淀,于是证明变质的过氧化钠粉末中有NaOH。老师对小明的设计提出了质疑,原因是。3.比较与分析归纳会使你的头脑变得更聪明。请分析下表中信息,回答有关问题:名称符号原子结构示意图单质化学式常温常压下状态单质与氢气反应氟FF2黑暗处爆炸氯ClCl2气态光照爆炸溴BrBr2液态加热反应碘I固态持续加热缓慢反应⑴请把上述表中的空格补充完整。⑵①试归纳氟、氯、溴、碘的原子结构规律(答一点即可):;②试归纳氟、氯、溴、碘对应单质的性质变化规律(答一点即可):;⑶已知:Cl2和Br2的化学性质相似,Cl2+H2O=HCl+HClO,其中HClO也是一种酸,它与氢氧化钠溶液反应的反应方程式为:HClO+NaOH=NaClO+H2O,试分别写出Br2与水,Br2与NaOH溶液反应的化学方程式:;。(4)与金属的置换反应规律相同,非金属单质与盐反应也有类似的规律。根据下列反应:Cl2+2NaBr=2NaCl+Br2、Br2+2KI=2KBr+I2。回答下列问题:(1)Cl2、Br2、I2的活泼性由弱到强的顺序是。(2)下列化学反应能发生的是(填序号)①2NaCl+I2=2NaI+Cl2②2KI+Cl2=2KCl+I2(3)查阅资料知硫的活泼性比上述三种单质都弱。请用一个化学方程式证明此结论。4.化学小组发现一袋包装破损的漂白粉,同学们对漂白粉其漂白作用是否失效产生了疑问。(当有效成分完全消失时,则漂白粉就完...