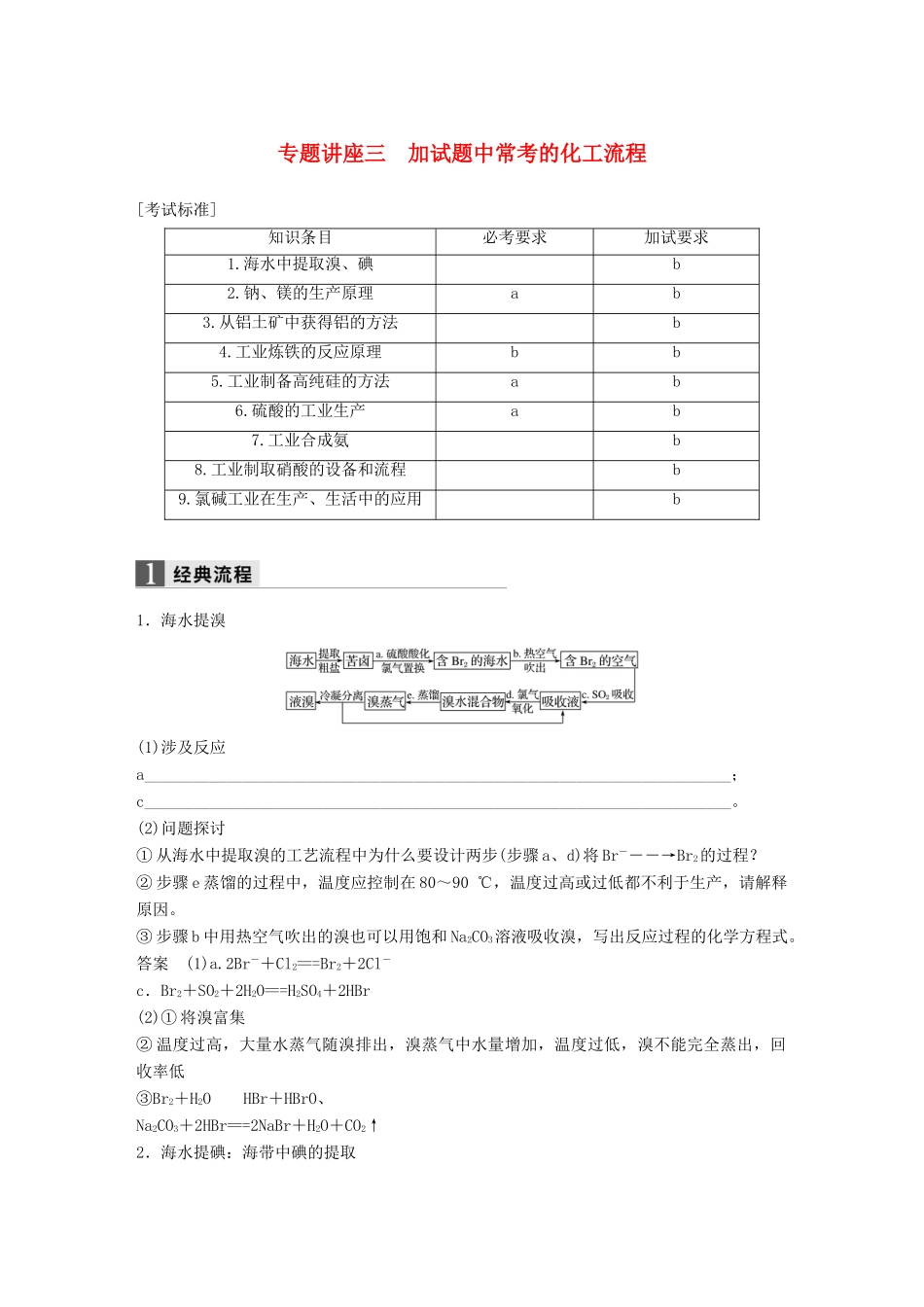
专题讲座三加试题中常考的化工流程[考试标准]知识条目必考要求加试要求1
海水中提取溴、碘b2
钠、镁的生产原理ab3
从铝土矿中获得铝的方法b4
工业炼铁的反应原理bb5
工业制备高纯硅的方法ab6
硫酸的工业生产ab7
工业合成氨b8
工业制取硝酸的设备和流程b9
氯碱工业在生产、生活中的应用b1.海水提溴(1)涉及反应a________________________________________________________________________;c________________________________________________________________________
(2)问题探讨①从海水中提取溴的工艺流程中为什么要设计两步(步骤a、d)将Br-――→Br2的过程
②步骤e蒸馏的过程中,温度应控制在80~90℃,温度过高或过低都不利于生产,请解释原因
③步骤b中用热空气吹出的溴也可以用饱和Na2CO3溶液吸收溴,写出反应过程的化学方程式
答案(1)a
2Br-+Cl2===Br2+2Cl-c.Br2+SO2+2H2O===H2SO4+2HBr(2)①将溴富集②温度过高,大量水蒸气随溴排出,溴蒸气中水量增加,温度过低,溴不能完全蒸出,回收率低③Br2+H2OHBr+HBrO、Na2CO3+2HBr===2NaBr+H2O+CO2↑2.海水提碘:海带中碘的提取(1)涉及反应:c_______________________________________________________________
(2)问题探讨①步骤a灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(从下列仪器中选出所需的仪器,将标号字母填写在空白处)
A.烧杯B.坩埚C.表面皿D.泥三角E.酒精灯F.干燥器②步骤e的目的是从含碘苯溶液中