高三复习专题讲座-元素化合物——碳、硅及新型无机非金属材料一、本讲教学进度及主要内容第三部分元素化合物——碳、硅及新型无机非金属材料主要内容:1.构建碳、硅元素的知识网络2.掌握两种元素对应的单质,氧化物、酸及其盐的重要性质3.了解硅酸盐工业和新型无机非金属材料二、学习指导(一)构建知识网络一方面抓住典型物质作为核心,尽可能向外发散和向内收效,甚至可扩展到相关的有机知识,另方面要区分条件的不同(如温度、用量、酸碱性等),尽量分类整理,做到有序存档
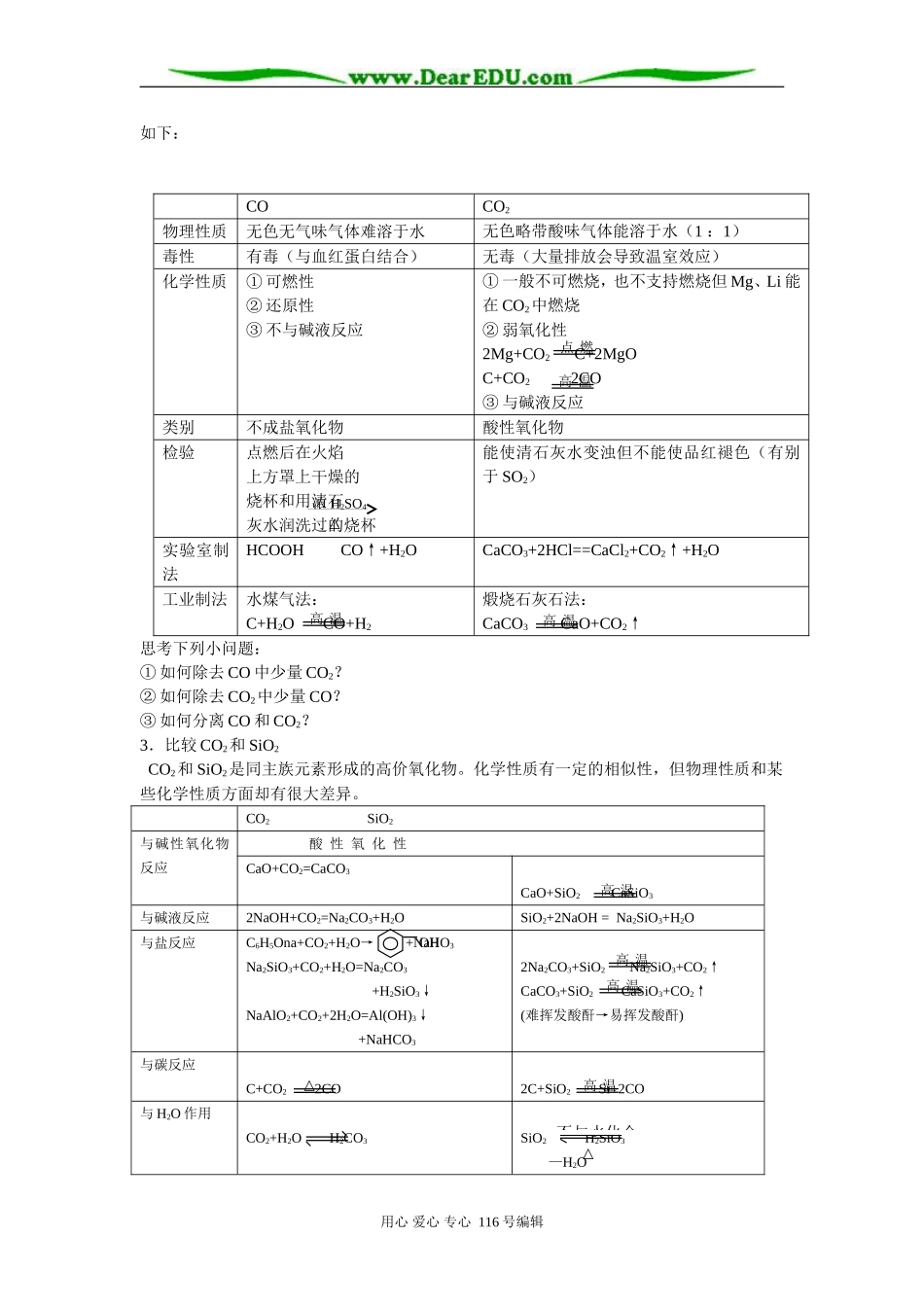
1.碳元素及其化合物的转化用心爱心专心116号编辑C2H2O2H2O高温高温△△2.硅元素及其化合物的转化(二)典型构质的性质1.单质碳C原子间结合方式(1)同素异形体的多样性分子中所含C原子数不同金刚石——原子晶体原子晶体石墨——混合晶体分子晶体(2)活性炭的重要性质和作用↓多孔疏松结构→吸附力强→吸附气体或溶液里的某些有色物质
↓实例①去臭气——吸附水中有臭味物质(净化水)②漂白——吸附某些食物和工业产品中的色素③去毒——吸附有毒气体(如NO2、Cl2等)(用于防毒面具)(3)碳的化学性质常温:稳定加热、高温或点燃:常表现还原性,作还原剂一般加热时,C→CO2高温时,C→CO如:C+H2OCO+H22C+SiO22CO+SiC+2CuO2Cu+CO2C+4HNO3(浓)CO2↑+4NO2↑+2H2O想一想:为什么木炭燃烧时无火焰
2.碳的氧化物CO、CO2尽管用为碳的氧化物,但是两者的物理性质,化学性质均有较大区别,可列表比较用心爱心专心116号编辑高温点燃浓H2SO4△高温高温高温高温高温高温△+H2O△OH如下:COCO2物理性质无色无气味气体难溶于水无色略带酸味气体能溶于水(1:1)毒性有毒(与血红蛋白结合)无毒(大量排放会导致温室效应)化学性质①可燃性②还原性③不与碱液反应①一般不可燃烧,也不支持燃烧但Mg、Li能在C