第二章p区元素(一)§2
3碳族元素§2
2硼族元素§2
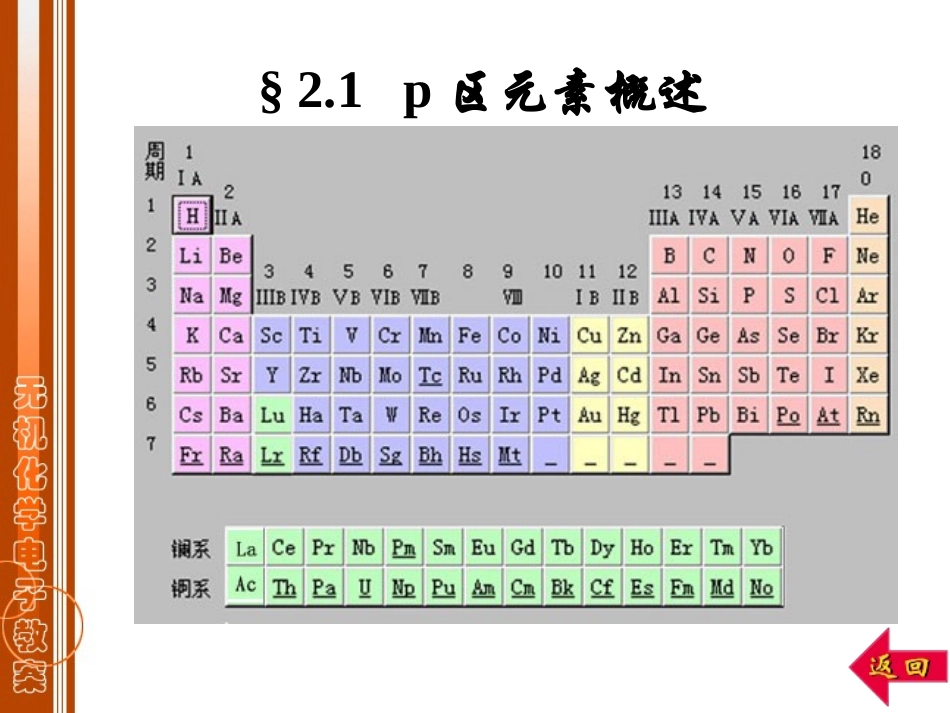
1p区元素概述§2
4氮族元素§2
1p区元素概述①第二周期元素具有反常性(只有2s,2p轨道)形成配合物时,配位数最多不超过4;第二周期元素单键键能小于第三周期元素单键键能(kJ/mol-1)E(N-N)=159E(O-O)=142E(F-F)=141E(P-P)=209E(S-S)=264E(Cl-Cl)=199p区元素性质的特征•各族元素性质由上到下呈现二次周期性②第四周期元素表现出异样性(d区插入)EV458
1)/ClClO(23V513
1)/BrBrO(23EV209
1)/IIO(23EV226
1)/ClOClO(34E例如:溴酸、高溴酸氧化性分别比其他卤酸(HClO3,HIO3)、高卤酸(HClO4,H5IO6)强
1)/IOIOH(365EV763
1)/BrOBrO(34③最后三个元素性质缓慢地递变K+Ca2+Ga3+Ge4+As5+r/pm13399625347Rb+Sr2+In3+Sn4+Sb5+r/pm148113817162Cs+Ba2+Tl3+Pb4+Bi5+r/pm169135958474(d区、f区插入)价电子构型:ns2np1-5例如:氯的氧化值有+1,+3,+5,+7,-1,0等
惰性电子对效应:同族元素从上到下,低氧化值化合物比高氧化值化合物变得更稳定
•多种氧化值例如:Si(II)Pb(IV)价电子结构分别为[Xe]6s2,[Xe]•电负性大,形成共价化合物§2
2硼族元素2
4铝的化合物2
3硼的化合物2
2硼族元素的单质2
1硼族元素概述2
1硼族元素概述硼族(ⅢA):B,Al,Ga,In,Tl价电子构型:ns2np1缺电子元素:价电子数