第三章p区元素(二)§3
1氧族元素§3
3P区元素化合物性质的递变规律§3
1氧族元素3
3硫及其化合物3
2氧及其化合物3
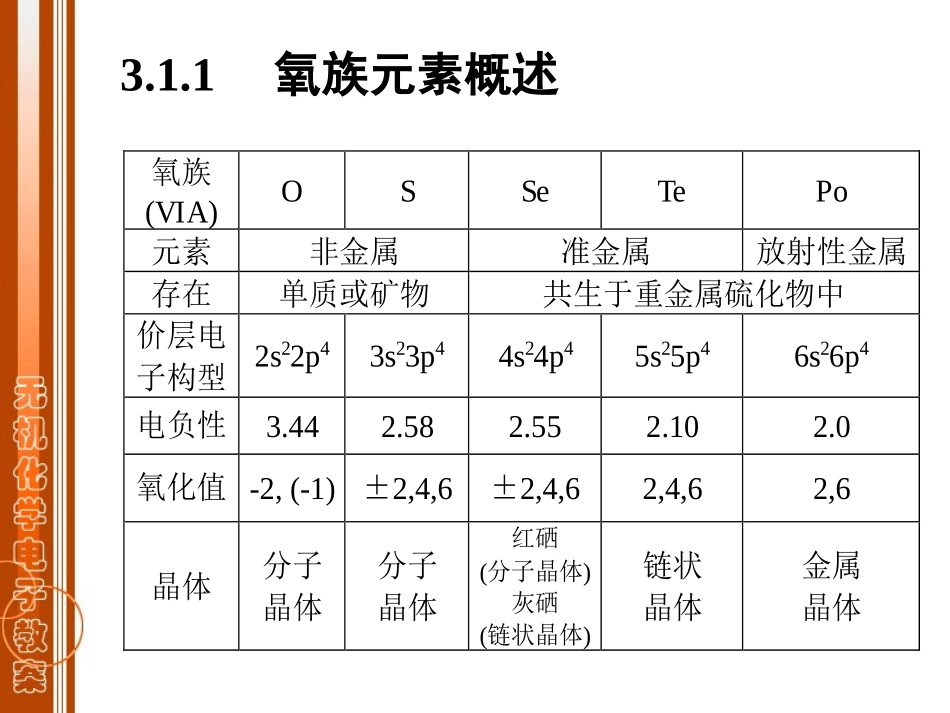
1氧族元素概述氧族(VIA)OSSeTePo元素非金属准金属放射性金属存在单质或矿物共生于重金属硫化物中价层电子构型2s22p43s23p44s24p45s25p46s26p4电负性3
0氧化值-2,(-1)±2,4,6±2,4,62,4,62,6晶体分子晶体分子晶体红硒(分子晶体)灰硒(链状晶体)链状晶体金属晶体3
1氧族元素概述氧O(Oxygen):存在形式O2(大气圈)、H2O(水圈)、SiO2及硅酸盐,其它含氧化合物(岩石圈)
6%,居第1位;氧族元素的存在形式氧族元素的存在形式钋Po(Polonium):放射性元素,本章不做介绍
硒Se(Selenium):硒铅矿PbSe,硒铜矿CuSe;碲Te(Tellurium):碲铅矿PbTe;硫S(Sulfur):天然单质硫矿;硫化物矿
方铅矿PbS,闪锌矿ZnS;硫酸盐矿:石膏CaSO4·2H2O,芒硝Na2SO4·10H2O,重晶石BaSO4,天青石SrSO4,占0
048%居第16位;H2RH2OH2SH2SeH2Te化学活性:小大稳定性:大小酸性:弱强熔沸点:最高小大单质Se单质Te碱性:2242222222s2121)(π)(π)()()()()(p*pps*s*sσσσσσ1
氧(O2)分子轨道电子排布式:3
2氧及其化合物OO酸性:(氧化性强)0
401VE4OH4eO2HO--221
229VEO2H4e4HO2-2氧的制备主要从空气中和H2O制氧:97%是从空气中提取的,3%是电解水制取的
工业法:液化空气,分馏制氧,压入钢瓶中储存:纯度:99
5%实验室制氧2KClO3=