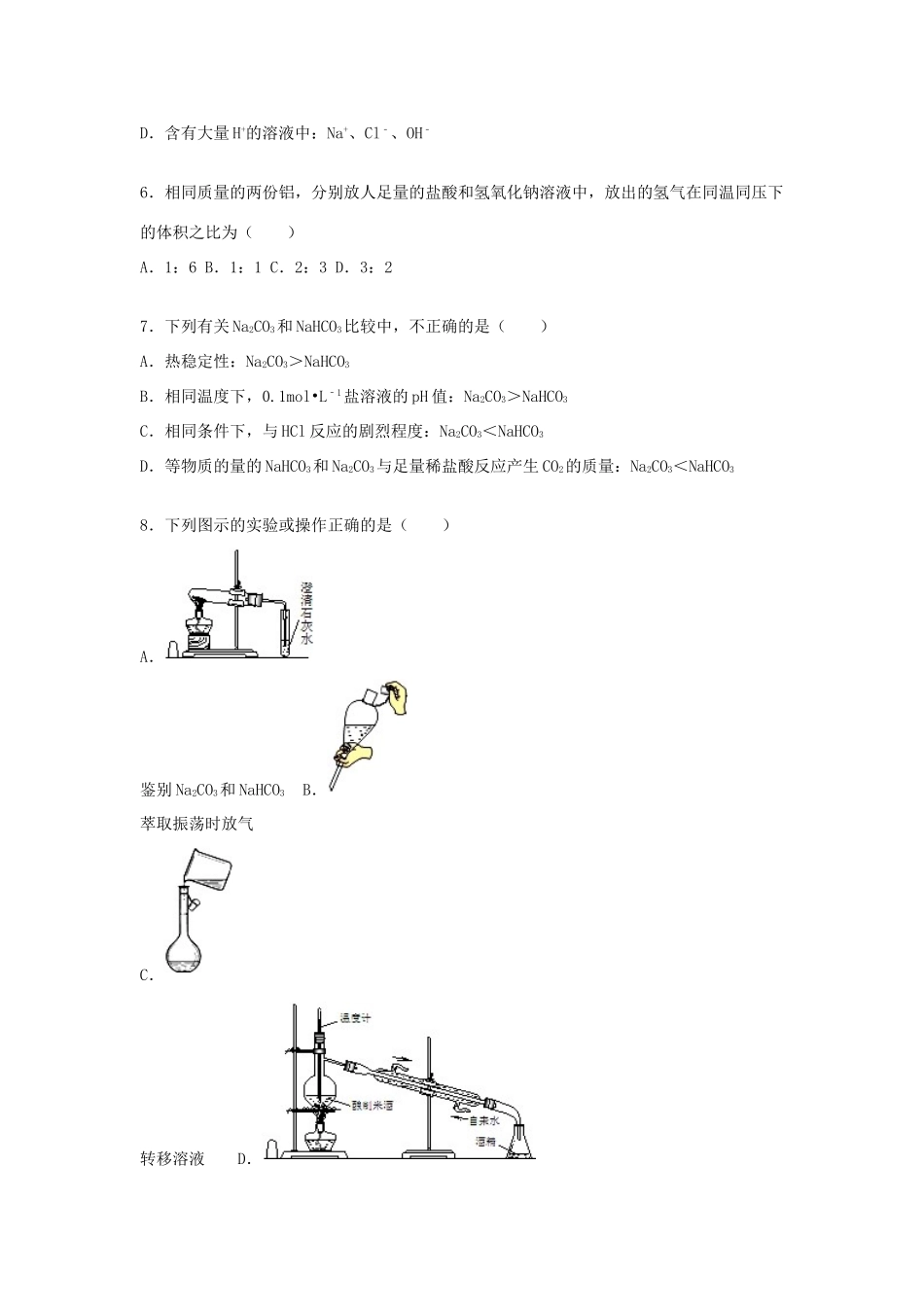
2015-2016学年广东省梅州市兴宁一中高一(上)第二次月考化学试卷一、单选题(本题包括14小题,每小题3分,共42分)1.下列关于金属元素特征的叙述正确的是()A.金属元素的原子只有还原性,离子只有氧化性B.金属元素在化合物中一定显正价C.金属元素在不同化合物中化合价均不同D.金属元素所有单质在常温下均为固体2.下列有关物质用途的叙述,错误的是()A.氧化钠可用作漂白剂B.明矾可用作净水剂C.碳酸氢钠可用于治疗胃酸过多D.氧化铝可用来制造耐火坩埚3.下列分离混和物的实验计划中不正确的是()A.分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)﹣﹣蒸馏B.从含有少量NaCl的KNO3溶液中提取KNO3﹣﹣热水溶解、降温结晶、过滤C.从水中分离出碘的CCl4溶液﹣﹣用分液漏斗分液D.将溴水中的溴转移到有机溶剂中﹣﹣加入酒精萃取4.下列离子方程式正确的是()A.碳酸钙和盐酸反应:CO32﹣+2H+═H2O+CO2↑B.向硝酸银溶液中加盐酸:Ag++C1﹣═AgCl↓C.向稀盐酸溶液中加铁:3Fe+6H+═3Fe3++3H2↑D.向氢氧化钡溶液中加硫酸溶液:Ba2++SO42﹣═BaSO4↓5.在下列各溶液中,离子一定能大量共存的是()A.无色溶液中:Na+、Cu2+、Cl﹣B.能与金属铝反应放出氢气的溶液中:K+、CO32﹣、NH4+C.能使酚酞试液变红的溶液中:Na+、Cl﹣、SO42﹣D.含有大量H+的溶液中:Na+、Cl﹣、OH﹣6.相同质量的两份铝,分别放人足量的盐酸和氢氧化钠溶液中,放出的氢气在同温同压下的体积之比为()A.1:6B.1:1C.2:3D.3:27.下列有关Na2CO3和NaHCO3比较中,不正确的是()A.热稳定性:Na2CO3>NaHCO3B.相同温度下,0.1mol•L﹣1盐溶液的pH值:Na2CO3>NaHCO3C.相同条件下,与HCl反应的剧烈程度:Na2CO3<NaHCO3D.等物质的量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的质量:Na2CO3<NaHCO38.下列图示的实验或操作正确的是()A.鉴别Na2CO3和NaHCO3B.萃取振荡时放气C.转移溶液D.用酿制的米酒获取酒精9.反应条件与环境对化学反应会产生影响,下列错误的是()化学反应影响因素AH2O2不稳定,向溶液中加入少量MnO2后的分解速率明显加快催化剂BNa与O2反应既能生成Na2O也能生成Na2O2温度C20mL双氧水比10mL双氧水产生更多的氧气浓度D过氧化氢在酸、碱、中性条件下将高锰酸钾分别还原成Mn2+、MnO42﹣、MnO2溶液的酸碱性A.AB.BC.CD.D10.“混盐”是指一种金属离子与多种酸根离子构成的盐,如CaOCl2就是一种混盐.“复盐”是指含有多种简单阳离子和一种酸根阴离子的盐,如KAl(SO4)2就是一种复盐.下列各化合物中属于混盐的是()A.Ca(NO3)ClB.(NH4)2Fe(SO4)2C.NaHCO3D.K3[Fe(CN)6]11.设阿伏加德罗常数的值为NA,则下列说法正确的是()A.1molNa2O2中阴、阳离子的总数是4NAB.常温常压下,11.2LCO2所含的原子数为1.5NAC.标准状况下,54gH2O中含有分子数为3NAD.1mol/L的MgCl2溶液中Cl﹣离子数为2NA12.下列关于氧化还原反应的叙述中,正确的是()A.有单质参加的反应一定是氧化还原反应B.一种物质被氧化,必有另一种物质被还原C.化学反应中,Mg失去2个电子,Al失去3个电子,因此还原性:Al>MgD.2Fe+3Cl22FeCl3;Fe+SFeS由此可以判断氧化性:Cl2>S13.关于KClO3+6HCl3Cl2↑+KCl+3H2O反应,以下说法正确的是()A.Cl2是氧化产物,KCl是还原产物B.还原剂与氧化剂的物质的量之比为6:1C.1molKClO3参加反应,转移5mol电子D.反应有单质生成,所以是置换反应14.某学小组同学设计了以下三组实验验证某无色溶液中含有的离子.下列说法正确的是()(1)溶液直接观察无明显的紫色火焰:证明没有K+(2)溶液产生白色沉淀:证明有SO42﹣(3)溶液白色沉淀无色溶液白色沉淀:证明有Al3+.A.该无色溶液不可能是明矾溶液B.这三组实验中,只有(3)是严密合理的C.步骤④的离子方程式为:Al3++3OH﹣=Al(OH)3↓D.步骤⑥的化学方程式为:NaAlO2+H2O+CO2=Al(OH)3↓+NaHCO3二、填空题.15.按要求填空(1)铁与水蒸气反应:(写出化学方程式)(2)氧化铝与氢氧化钠溶液反应:(写出离子方程式)(3)NaHCO3与少量Ca(OH)2溶液反应:(写出离子方程式).16.某待...