2025年2月10日第一章化学反应与能量一、燃烧热1
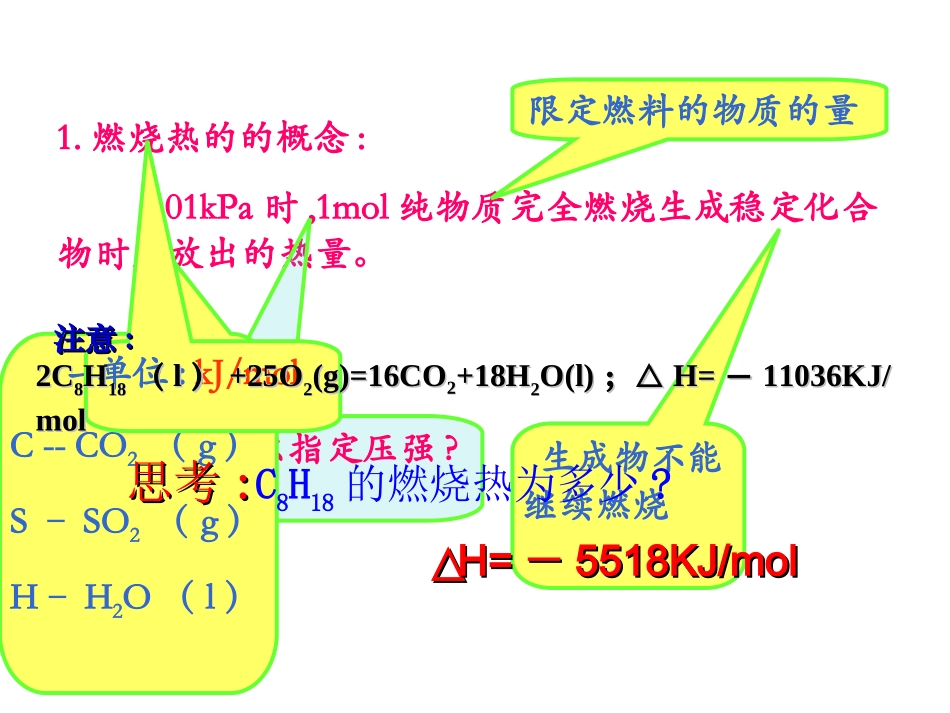
燃烧热的的概念:101kPa时,1mol纯物质完全燃烧生成稳定化合物时所放出的热量
为什么指定压强
生成物不能继续燃烧一般指:C--CO2(g)S–SO2(g)H–H2O(l)单位:kJ/mol限定燃料的物质的量注意注意::2C2C88HH1818((ll))+25O+25O22(g)=16CO(g)=16CO22+18H+18H22O(l)O(l);△;△H=H=--11036KJ/11036KJ/molmol思考思考::C8H18的燃烧热为多少
△△H=H=--5518KJ/mol5518KJ/mol2
表示的意义:如:CH4的燃烧热为890
3KJ/mol
含义:在101KPa时,1molCH4完全燃烧时,放出890
3KJ的热量
表示燃烧热的热化学方程式的书写:应以应以1mol1mol物质的标准来配平其余物质的化物质的标准来配平其余物质的化学计量数学计量数((常出现分数常出现分数))4
一定量可燃物完全燃烧时放出的热量QQ放放=n(=n(可燃物可燃物))ⅹⅹ︱︱△△HH︱︱CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890
31KJ/mol燃烧热与中和热的区别与联系相同点燃烧热中和热能量变化放热反应ΔHΔH