考点专练23化学平衡状态及其移动两年高考真题演练1
(2014·江苏化学,15)一定温度下,在三个体积均为1
0L的恒容密闭容器中发生反应:2CH3OH(g)CH3OCH3(g)+H2O(g)容器编号温度/℃起始物质的量(mol)平衡物质的量(mol)CH3OH(g)CH3OCH3(g)H2O(g)Ⅰ3870
080Ⅱ387040Ⅲ2070
090下列说法正确的是(双选)()A.该反应的正反应为放热反应B.达到平衡时,容器Ⅰ中的CH3OH体积分数比容器Ⅱ中的小C.容器Ⅰ中反应到达平衡所需时间比容器Ⅲ中的长D.若起始时向容器Ⅰ中充入CH3OH0
15mol、CH3OCH30
15mol和H2O0
10mol,则反应将向正反应方向进行2.[2015·广东理综,31(2)(3)(4)]用O2将HCl转化为Cl2,可提高效益,减少污染
(1)新型RuO2催化剂对上述HCl转化为Cl2的总反应[2HCl(g)+O2H2O(g)+Cl2(g)ΔH]具有更好的催化活性,①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的αHCl~T曲线如下图:则总反应的ΔH________0(填“>”、“=”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是________
②在上述实验中若压缩体积使压强增大,画出相应αHCl~T曲线的示意图,并简要说明理由____________________________________
③下列措施中,有利于提高α(HCl)的有________
A.增大n(HCl)B.增大n(O2)C.使用更好的催化剂D.移去H2O(2)一定条件下测得反应过程中n(Cl2)的数据如下:t/min02
0n(Cl2)/10-3mol01
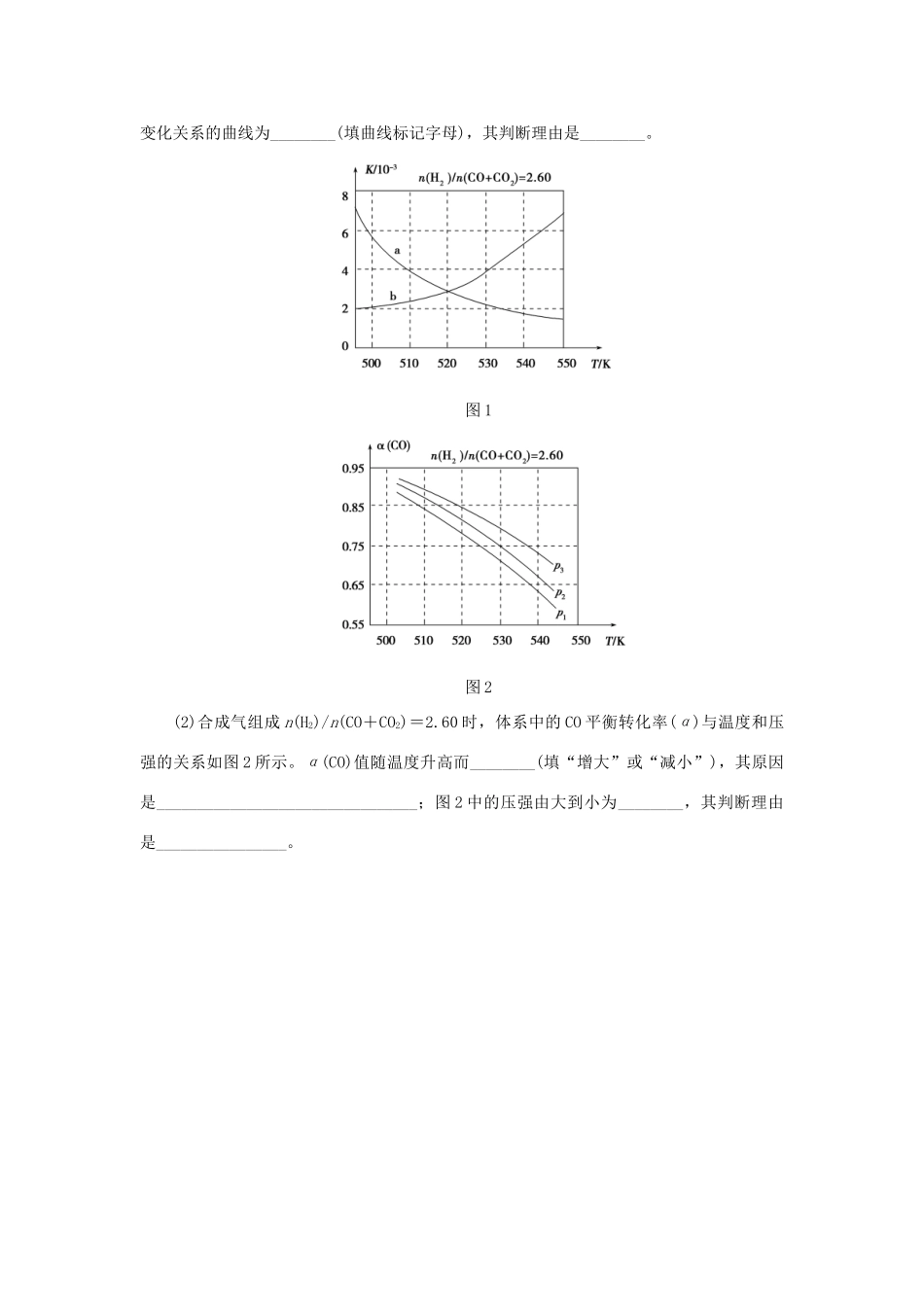
0min内以HCl的物质的量