高一化学碱金属的综合提高【本讲主要内容】碱金属的综合提高复习《碱金属》的原子结构、单质及化合物的性质,用途
通过《碱金属》的复习,学会元素及化合物特别是金属元素的知识的复习归纳方法和知识的内在联系及规律
通过《碱金属》的复习,学会建立化学知识的结构和网络体系
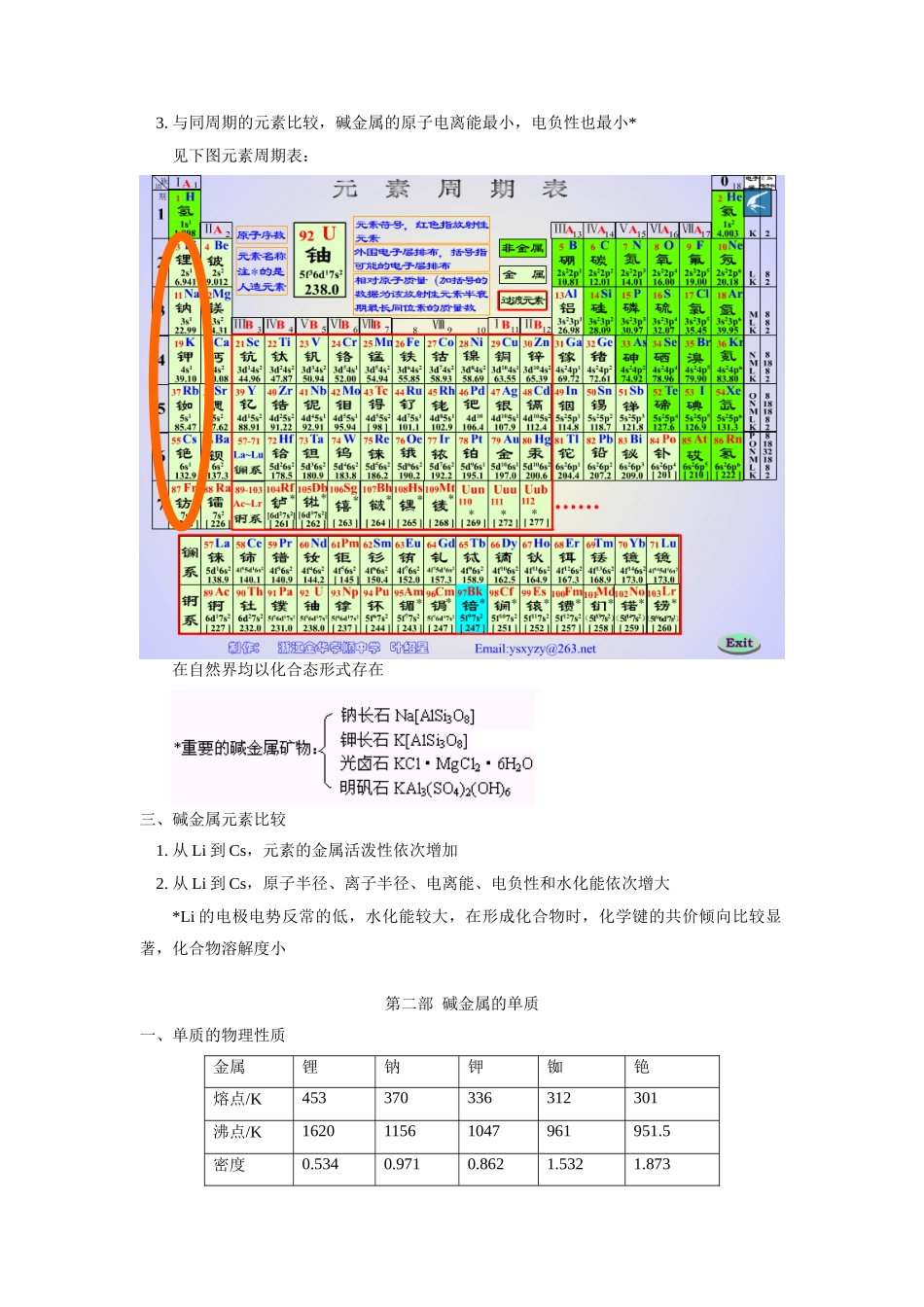
培养分析、归纳、对比、总结及创新的能力,培养逻辑思维能力【知识掌握】【知识点精析】前面我们学习了金属钠及其化合物和碱金属元素的相关知识,这是同学们在高中学习的第一个金属元素族
通过这一族的学习,我们应该初步了解族元素学习的方法,即:重点掌握代表物质的性质,其他元素的性质可以利用相似性和递变性的规律加以掌握
这样就可把所学知识形成结构的网络,把分散的内容统一起来,为以后学习典型的非金属元素族——卤族铺平道路,使得元素周期表和元素周期律的学习“水到渠成”
下面我们就分别总结一下第一部分碱金属的通性一、包含元素:锂、钠、钾、铷、铯二、碱金属的通性1
与同周期的元素比较,碱金属元素总是最活泼的金属元素2
与同周期的元素比较,碱金属的原子半径最大3
与同周期的元素比较,碱金属的原子电离能最小,电负性也最小*见下图元素周期表:在自然界均以化合态形式存在三、碱金属元素比较1
从Li到Cs,元素的金属活泼性依次增加2
从Li到Cs,原子半径、离子半径、电离能、电负性和水化能依次增大*Li的电极电势反常的低,水化能较大,在形成化合物时,化学键的共价倾向比较显著,化合物溶解度小第二部碱金属的单质一、单质的物理性质金属锂钠钾铷铯熔点/K453370336312301沸点/K162011561047961951
873硬度0
均具有银白色光泽2
具有良好的导电性3
硬度小,质软4
钠、钾是动物体必须的元素,是体液的重要成分二、单质的化学性质1
易与活泼的非金属单质