第三单元化学能与电能的转化第三单元化学能与电能的转化在容器中加入约2/3容积的稀硫酸,请按下列要求实验并记录实验现象:1
将一块铜片和一块锌片分别插入盛有稀硫酸的烧杯中
将一块铜片和一块锌片同时插入盛有稀硫酸的烧杯中
(铜片和锌片不要接触)3
用导线把锌片和铜片连接起来,插入盛有稀硫酸的烧杯中
在锌片和铜片的导线中间连接一个灵敏电流计,插入盛有稀硫酸的烧杯中
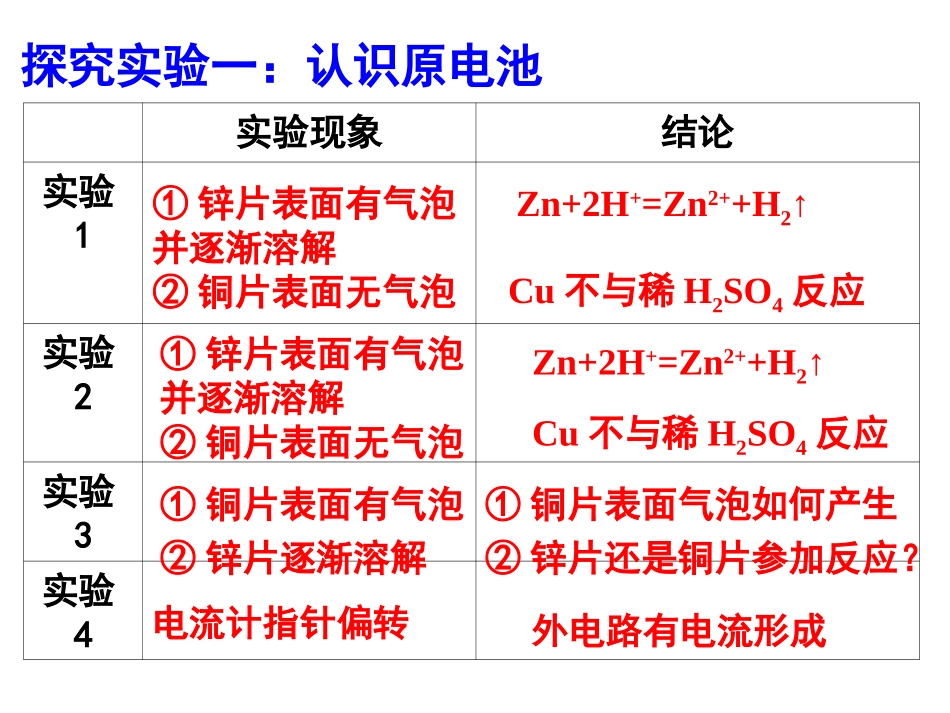
探究实验一:认识原电池实验现象结论实验1实验2实验3实验4①锌片表面有气泡并逐渐溶解②铜片表面无气泡①铜片表面有气泡②锌片逐渐溶解电流计指针偏转Zn+2H+=Zn2++H2↑Cu不与稀H2SO4反应外电路有电流形成①铜片表面气泡如何产生②锌片还是铜片参加反应
①锌片表面有气泡并逐渐溶解②铜片表面无气泡Zn+2H+=Zn2++H2↑Cu不与稀H2SO4反应负极正极Zn-2e-=Zn2+2H++2e-=H2还原剂(Zn)失去电子,发生氧化反应氧化剂(H+)在铜极上得到电子,发生还原反应还原剂失去的电子从锌极流出流入铜极
经外电路Zn2+H+SO42-电流方向1
原电池:将化学能转化成电能的装置装置化学能转化为电能原电池的原理:氧化还原反应2
原电池的电极反应电子锌片(负极):Zn-2e-=Zn2+(氧化反应)铜片(正极):2H++2e-=H2↑(还原反应)总反应Zn+2H+=Zn2++H2↑实验探究形成原电池的条件形成条件一:活泼性不同的两个电极负极:较活泼的金属正极:较不活泼的金属或非金属导体(石墨)等形成条件二:电极需插进电解质溶液中实验探究形成原电池的条件形成条件三:必须形成闭合回路实验探究形成原电池的条件实验探究形成原电池的条件形成条件四:必须存在自发的氧化还原反应3
构成原电池的条件(1)有活泼性不同的两个电极(2)两电极都接触电解质溶液(3)正极、负极、电解质溶液构成闭合回路(4)在电极表面上能发生自发