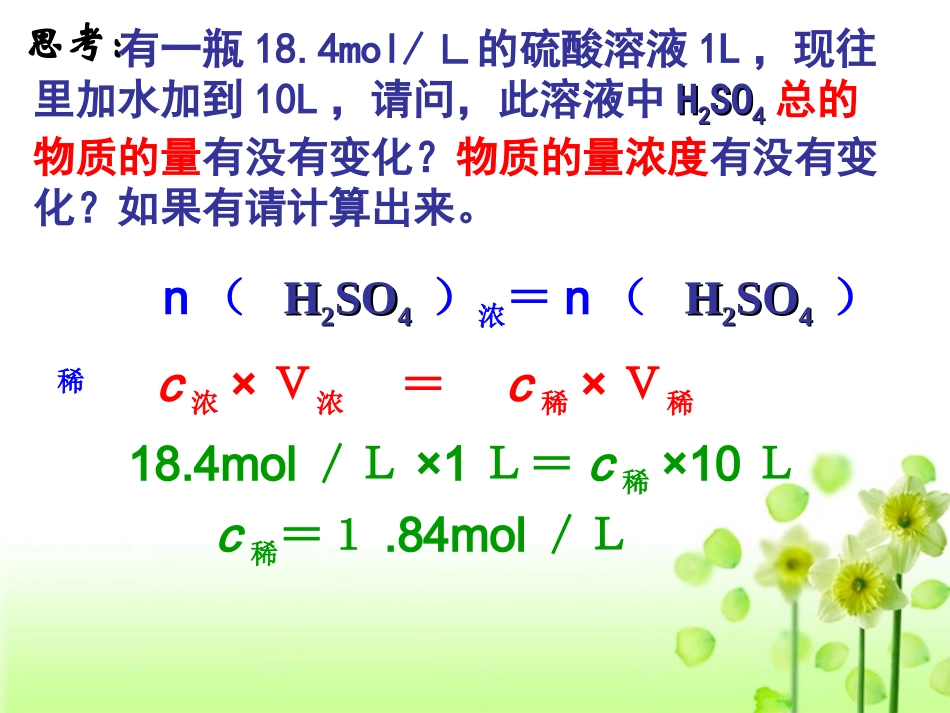
溶液的稀释及混合的计算思考:有一瓶18.4mol/L的硫酸溶液1L,现往里加水加到10L,请问,此溶液中HH22SOSO44总的物质的量有没有变化?物质的量浓度有没有变化?如果有请计算出来。n(HH22SOSO44)浓=n(HH22SOSO44)稀c稀=1.84mol/L18.4mol/L×1L=c稀×10Lc浓×V浓=c稀×V稀(1)一定物质的量浓度溶液的稀释例例11:配制:配制250mL1mol/LHCl250mL1mol/LHCl溶液,需要溶液,需要12mol/L12mol/LHClHCl溶液的体积是多少?溶液的体积是多少?解:设需要需要12mol/LHCl12mol/LHCl溶液的体积为溶液的体积为xx。。由CC((浓溶液浓溶液)·V()·V(浓溶液浓溶液))==CC((稀溶液稀溶液)·V()·V(稀溶液稀溶液))得得12mol/L··xx=1mol/L×0.250Lxx=0.0208L=20.8mL答:需要20.8mL12mol/LHCl12mol/LHCl溶液溶液。利用稀释前后溶质的物质的量相等C1V1=C2V2C1V1+C2V2=C3V3n1+n2=n3(2)不同浓度溶液混合的计算例2:5mol/L的盐酸溶液200L和2mol/L的盐酸溶液100L混合,求:混合后溶液中盐酸的物质的量浓度。(忽略混合时体积变化)混合前后溶质的物质的量总和不变5mol/L×0.200L+2mol/L×0.100L=x·(200+100)LX=X=4mol/L答:混合后HClHCl的物质的量浓度为的物质的量浓度为4mol/L4mol/L。•练习•名师一号P20第9题物质的量浓度与质量分数换算t℃时,NaCl的溶解度为Sg,溶液的密度为ρg/mL,求该溶液的质量分数及物质的量浓度n(NaCI)=M(NaCI)SV==mL(S+100)gρg/mL(S+100)ρc(NaCI)==mol/Ln(NaCI)V1000Sρ58.5(S+100)1000ρ(S+100)=Lt℃,100g水中溶解Sg的NaCl,形成g饱和溶液100+S求98%的H2SO4(密度为1.84g/mL)的物质的量浓度解:解:1L1L浓硫酸的质量:浓硫酸的质量:m(Hm(H22SOSO44))==ρ[HH22SOSO44(aq)]·V[HH22SOSO44(aq)]·ω(Hω(H22SOSO44))==1.84g/mL×1000mL×98%×1000mL×98%1.84×1000×98%g98g/mol=18.4moln(H2SO4)=因为因为1000mL1000mL浓硫酸中含浓硫酸中含18.4mol18.4molH2SO4,,浓硫酸中H2SO4的物质的量浓度为18.4mol/L18.4mol/L。。H2SO4的物质的量:注意单位换算•溶质质量分数为w%,密度为ρg/mL的某溶液中,其溶质的物质的量浓度的表达式:c=Mw%1000•溶液中溶质的物质的量浓度c,溶液的密度ρg/mL,其质量分数的表达式:W%=%1001000cM物质的量浓度与质量分数的换算练习:名师一号P20第8题作业1、质量分数为36.5%的盐酸,密度1.19g/cm3,求其物质的量浓度。