第1课时离子键学习目标核心素养建构1
知道化学键的概念
了解离子键的概念和成因及离子化合物的概念
能用电子式表示简单的离子化合物
[知识梳理]一、离子键及离子化合物1
化学键(1)概念:物质中直接相邻的原子或离子之间存在的强烈的相互作用叫做化学键
(2)类型:离子键和共价键是两种常见的化学键
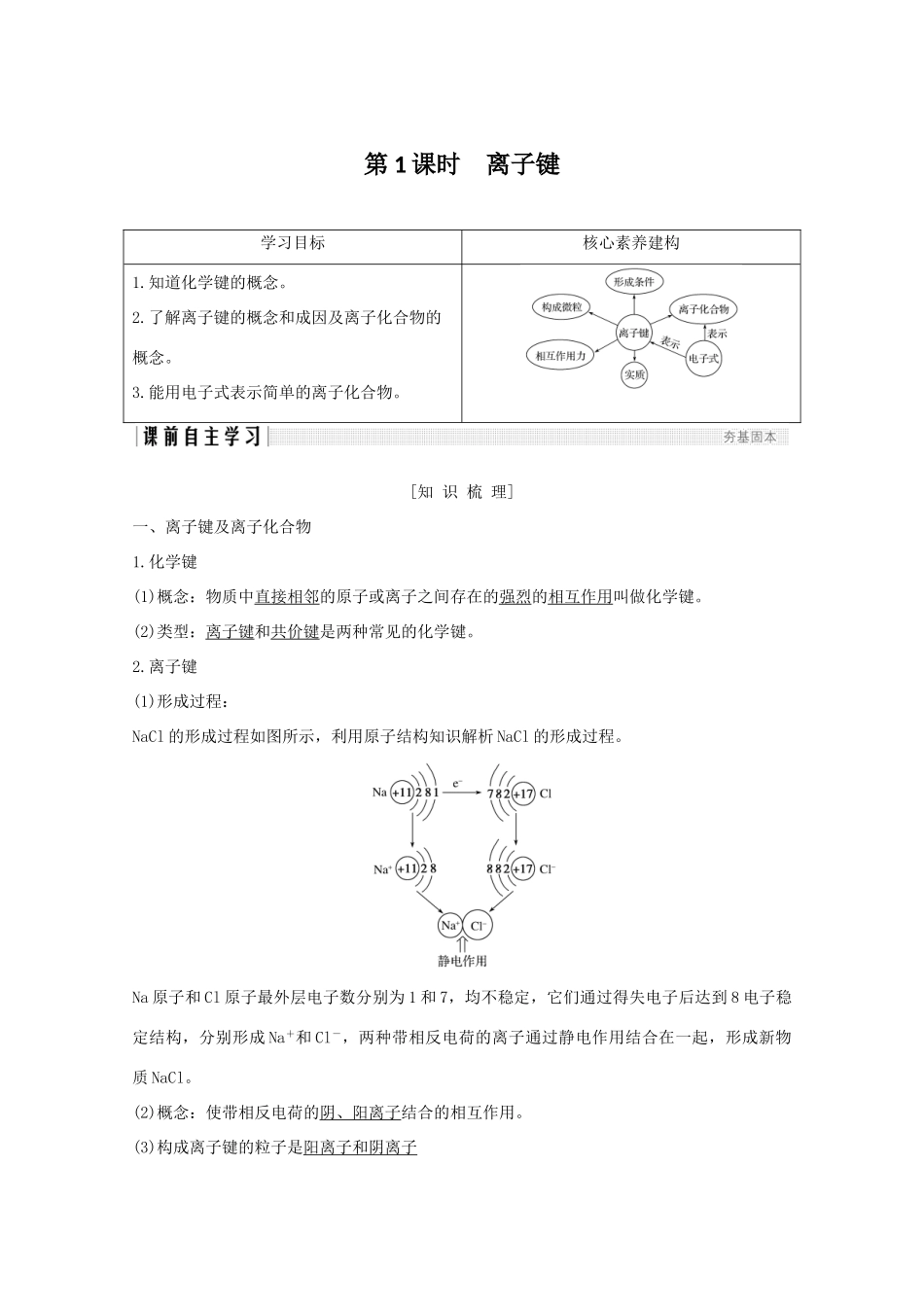
离子键(1)形成过程:NaCl的形成过程如图所示,利用原子结构知识解析NaCl的形成过程
Na原子和Cl原子最外层电子数分别为1和7,均不稳定,它们通过得失电子后达到8电子稳定结构,分别形成Na+和Cl-,两种带相反电荷的离子通过静电作用结合在一起,形成新物质NaCl
(2)概念:使带相反电荷的阴、阳离子结合的相互作用
(3)构成离子键的粒子是阳离子和阴离子(4)离子键的实质是静电作用
离子化合物(1)概念:由离子键构成的化合物
(2)常见的离子化合物的类型:①活泼金属氧化物:Na2O、MgO;②绝大多数盐:NaCl、K2SO4、CaCO3;③强碱:NaOH、Ba(OH)2
【自主思考】1
如何理解化学键的概念
常见的哪些元素易形成离子键
形成的过程是什么
提示活泼金属与活泼非金属元素原子易形成离子键,一般位于周期表中为ⅠA、ⅡA族的金属元素与ⅥA、ⅦA族的非金属元素
形成过程为:――→――→离子键3
如何理解离子键中的静电作用
提示静电作用包括静电吸引和静电排斥
静电吸引即阴、阳离子之间的相互吸引;静电排斥即原子核与原子核、核外电子与核外电子的排斥作用
二、电子式1
概念:由于在化学反应中,一般是原子的最外层电子发生变化,为了方便,我们在元素符号周围用“·”(小黑点)或“×”(叉号)表示原子或离子的最外层电子的式子叫做电子式
电子式的书写(1)原子的电子式:氢原子H·、钠原子Na·、氮原子、氯原子
(2)简单阳离子的电子式:简单阳离子是原子失去最外层电子后