第四节氨硝酸硫酸练习一()1.氨气可以做喷泉实验,这是利用A
极易溶于水D
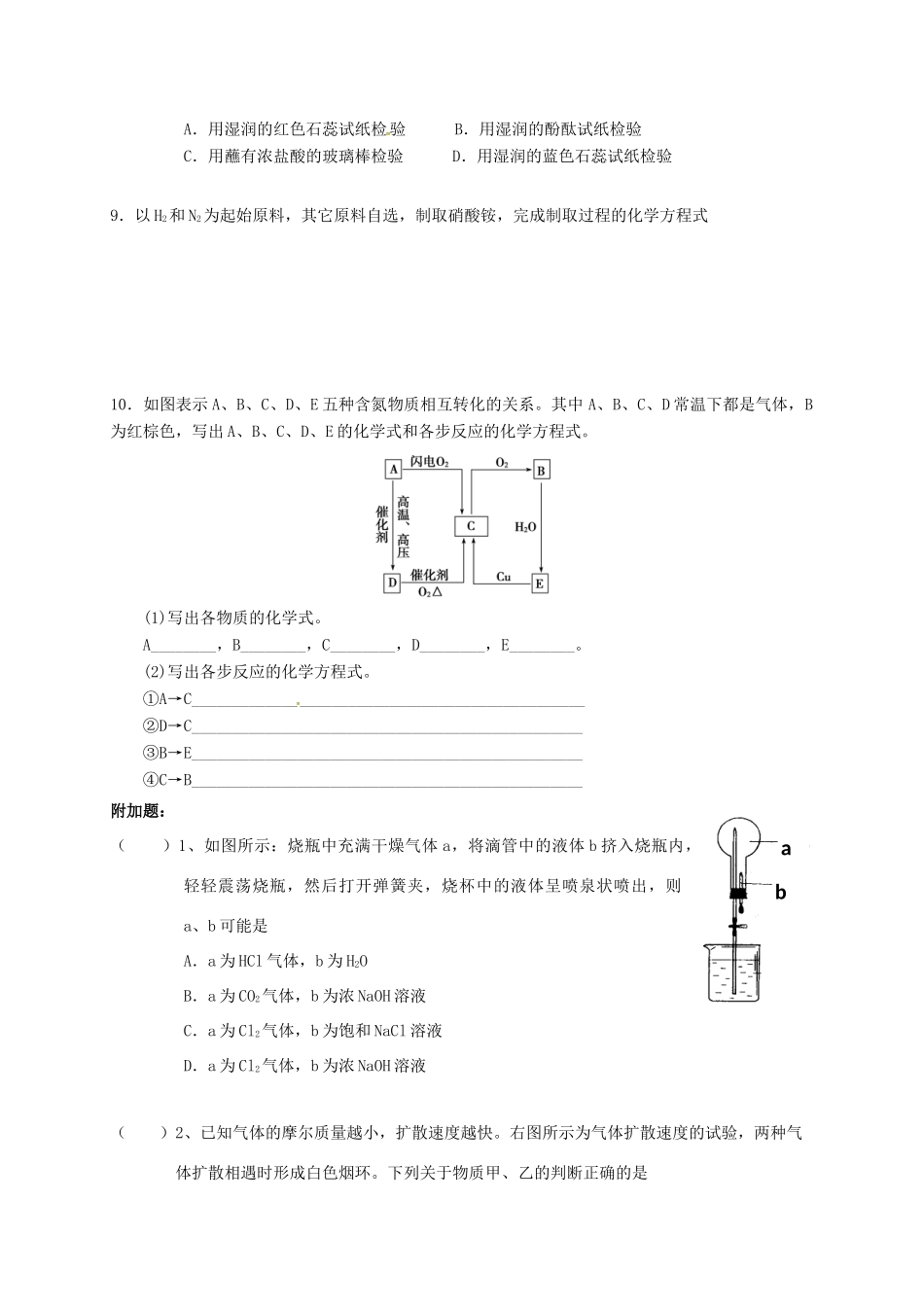
与水起反应()2.下列离子方程式错误的是A.氨气通入稀硫酸NH3+H+=NH4+B.稀烧碱溶液和氯化铵溶液混合NH4++OH-=NH3·H2OC.碳酸氨和浓烧碱溶液混合NH4++OH-=NH3↑+H2OD.Cl2和水反应Cl2+H2O=2H++Cl-+ClO-()3.四支试管分别充满O2、NO2、Cl2、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满Cl2的试管是()4.氨水显弱碱性的主要原因是A.通常状况下,氨的溶解度不大B.氨水中的NH3·H2O电离出少量的OH-C.溶于水的氨分子只有少量电离D.氨本身的碱性弱()5.关于氨的下列叙述中,错误的是A.氨易液化,因此可用来作制冷剂B.氨极易溶于水,因此可用来作喷泉实验C.氨极易溶解于水,因此氨水比较稳定(不容易分解)D.氨溶解于水显弱碱性,因此可使酚酞试剂变为红色()6.下列反应中,NH3既显还原性,又显碱性的是A.NH3+HClNH4ClB.2NH3=3H2+N2C.3CuO+2NH33Cu+N2+3H2OD.8NH3+3Cl26NH4Cl+N2()7.能把Na2SO3、NH4NO3、KCl、(NH4)2SO4四种无色溶液区别开的一种试剂是(必要是可加热)A.Ba(OH)2B.KOHC.NaOHD.AgNO3()8.下列检验氨气的方法不可行的是A.用湿润的红色石蕊试纸检验B.用湿润的酚酞试纸检验C.用蘸有浓盐酸的玻璃棒检验D.用湿润的蓝色石蕊试纸检验9.以H2和N2为起始原料,其它原料自选,制取硝酸铵,完成制取过程的化学方程式10.如图表示A、B、C、D、E五种含氮物质相互转化的关系
其中A、B、C、D常温下都是气体,B为红棕色,写出A、B、C、D、E的化学式和各步反应的化学方程式