高一化学化学能与电能的转化单元复习【教学目标】一知识与技能1.通过铜-锌原电池、惰性电极电解氯化铜溶液的模型的对比分析,初步认识原电池、电解池的原理、构成条件和能量转化方面的区别2.能够正确书写简单的原电池、电解池的电极反应
3.了解化学电源的应用,能够正确书写碱性氢氧燃料的电极反应(发展要求);4
了解电解原理的应用,能够正确书写惰性电极电解CuCl2溶液的电极反应式和反应方程式,书写饱和食盐水的方程式,判断电极产物
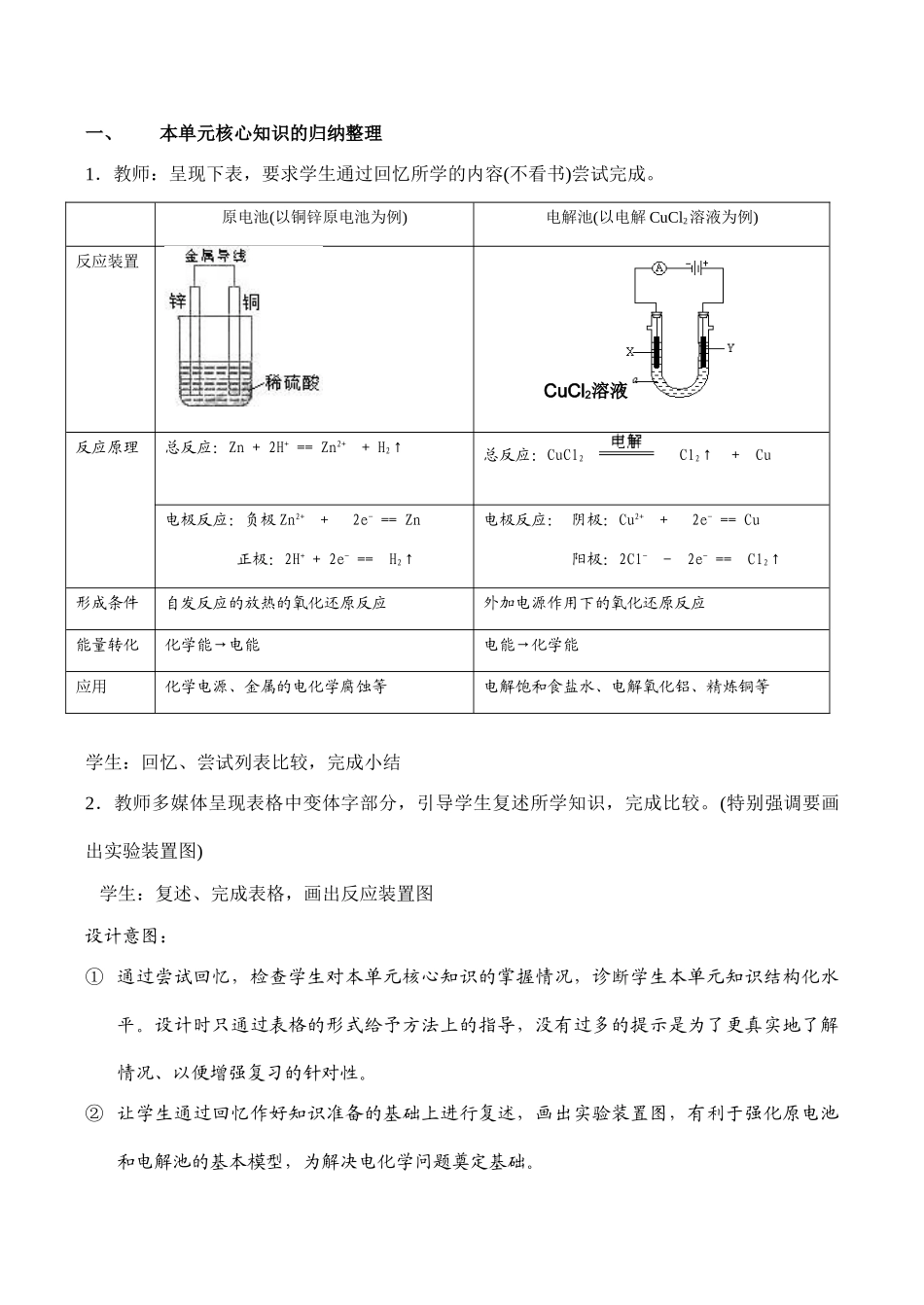
5.能够运用原电池原理设计简单的化学电池(发展要求)二、过程与方法1.通过对原电池、电解池的列表比较,学习比较归纳在知识结构化中的应用2.通过电化学问题的解决过程,了解常见电化学问题的解决策略三、情感态度价值观1.通过原电池、电解池的原理和反应装置的复习,整体上形成能量转化观2.通过原电池、电解池的原理的微观过程的分析,养成从微观变化观的视角认识物质世界变化的方式3.通过原电池和电解池在生活、生产中的应用,赞赏化学在促进人类社会发展中的巨大价值,丰富学生积极的化学情感【重点难点】重点:原电池、电极池的工作原理,电极反应式难点:原电池的工作原理及模型建构【教学模式】学案式自主复习【教学过程】主要教学环节如下一、本单元核心知识的归纳整理1.教师:呈现下表,要求学生通过回忆所学的内容(不看书)尝试完成
原电池(以铜锌原电池为例)电解池(以电解CuCl2溶液为例)反应装置反应原理总反应:Zn+2H+==Zn2++H2↑总反应:CuCl2Cl2↑+Cu电极反应:负极Zn2++2e-==Zn正极:2H++2e-==H2↑电极反应:阴极:Cu2++2e-==Cu阳极:2Cl--2e-==Cl2↑形成条件自发反应的放热的氧化还原反应外加电源作用下的氧化还原反应能量转化化学能→电能电能→化学能应用化学电源、金属的电化学腐蚀等电解饱和食盐水、电解氧化铝、精炼铜等学生:回忆、尝试