九年级化学铁的性质和钢铁的冶炼知识精讲一
本周教学内容铁的性质和钢铁的冶炼二
重点、难点1
了解铁的物理性质与实际生活的不同;2
掌握重要化学性质,总结变化过程中铁的化合价的变化;3
掌握生铁和钢的冶炼方法;4
掌握含杂物质的化学方程式的计算方法
具体内容本章的重点是围绕着铁
首先,我们需要掌握哪些铁的物理性质
其次,需掌握的化学性质有哪些
总结铁在化学反应中化合价的变化特点
再次,生铁和钢的冶炼:什么叫合金
铁的合金有哪些
铁矿石应掌握哪些
炼铁的原理和化学方程式
炼钢的原理和化学方程式
最后,常见金属大多数都是常识性了解的内容,那么,需掌握的是:哪些金属在空气中被氧化易形成一层致密的氧化物薄膜
钛这种金属广泛应用于航空和船舶制造的优点是什么
[例1]如图所示:取一团光亮无锈的铁丝,放入一只洁净试管的底部,将试管倒放在一个盛有水的烧杯里
数天后,能观察到的现象是______________答案:铁丝生锈,试管内水面上升1/5
解析:注意铁丝生锈需要的条件,以及由此引起的其他现象
[例2]将铁粉和铜粉的混合物20g,放入足量的硫酸铜溶液中,完全反应后的红色固体共22g,求原反应物中铜的质量分数
答案:30%解析:运用差量法
[例3]炼200吨含3%杂质的生铁,需要含85%氧化铁的赤铁矿石多少吨
答案:326
1t解析:含杂计算,带入化学方程式的应是纯净物的质量
[例4]含氧化铁70%的赤铁矿60t,再冶炼过程中铁损失2%,求:最终能炼出含杂质4%的生铁多少t
0t解析:利用分步运算,关键考虑损失问题
[例5]用含杂质的57%的铝矿石(主要成分为三氧化二铝)来提炼金属铝,若炼出3
6吨铝,需此矿石多少吨
8t解析:带杂计算,带入化学方程式的应是纯净物的质量
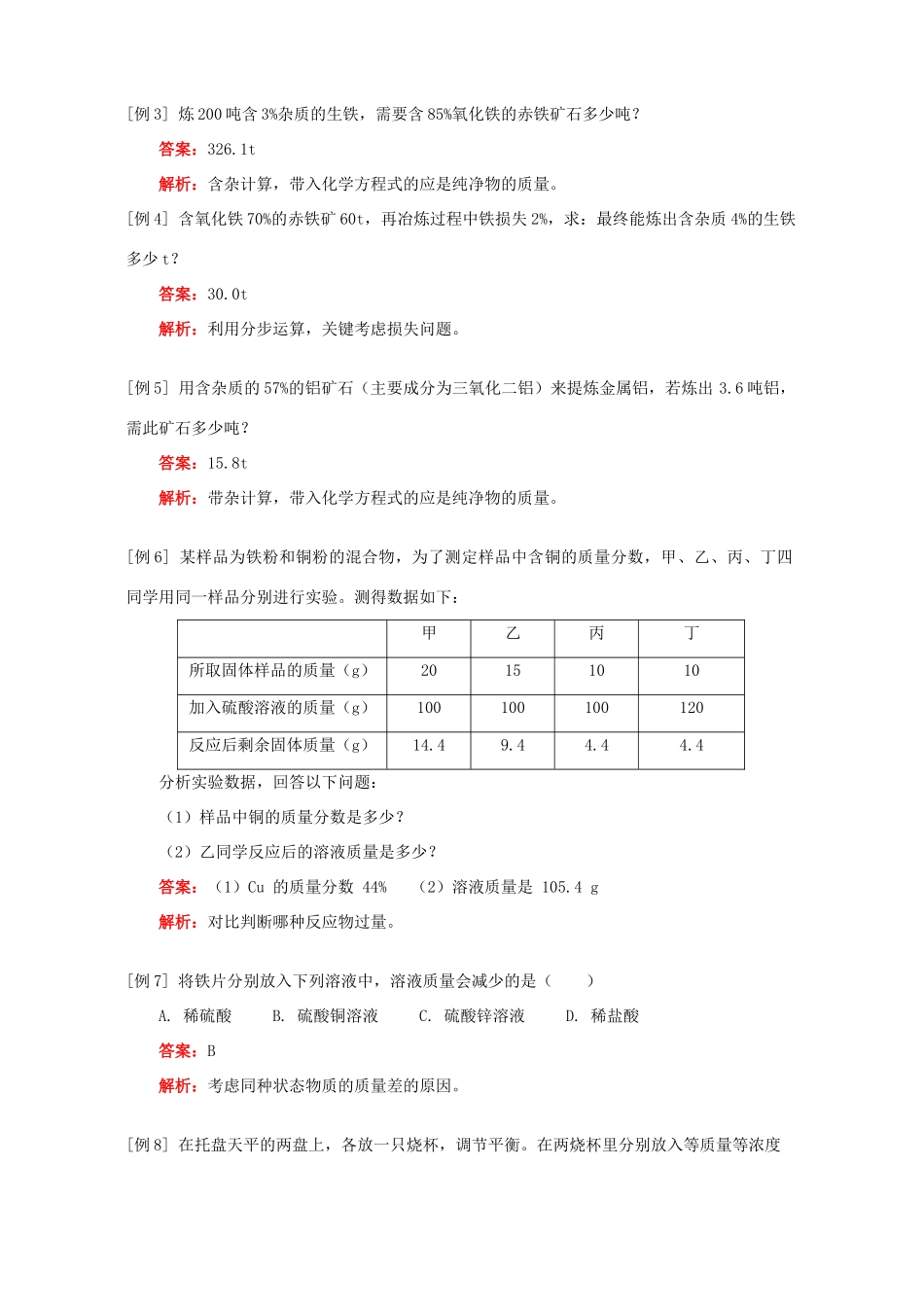
[例6]某样品为铁粉和铜粉的混合物,为了测定样品中含铜的质量分数,甲、乙、丙、丁