1/5元素周期律(讲义)一、知识点睛1
元素周期律元素的性质随着元素的递增而呈的变化,这个规律叫做元素周期律
微粒半径大小规律①同主族,从上到下原子半径逐渐
即电子层数越多,微粒的半径越
②同周期,从左到右原子半径逐渐(稀有气体除外)
即电子层数相同,核电荷数越大,原子的半径越
③电子层结构相同的离子,核电荷数越大,微粒半径越
(如FNa+Mg2+Al3+)④同种元素,原子半径阳离子半径;同种元素,原子半径阴离子半径
即对同一元素,价态越高半径越
(如:Fe2+Fe3+)3
主族元素化合价规律(1)最高正价数=主族序数=最外层电子数如:2、3周期主族元素的最高正价从+1到+7变化(O通常显负价,F没有正价)
(2)最低负价绝对值=8-主族序数(限ⅣA族~ⅦA族)如:2、3周期主族元素的负价从-4到-1变化(金属元素没有负价)
金属性和非金属性规律(1)同一周期元素,从左到右,原子失电子能力逐渐减弱、得电子能力逐渐增强,则金属性越来越,非金属性越来越
(2)同一主族元素,从上到下,原子失电子能力逐渐增强、得电子能力逐渐减弱,则金属性越来越,非金属性越来越
(3)金属性和非金属性应用①元素的金属性越强,单质与水(或酸)反应置换出氢越_,元素最高价氧化物对应的水化物的碱性越_
②元素的非金属性越强,单质与氢气化合越且生成的气态氢化物的稳定性越,元素最高价氧化物对应的水化物的酸性越
2/5二、精讲精练1
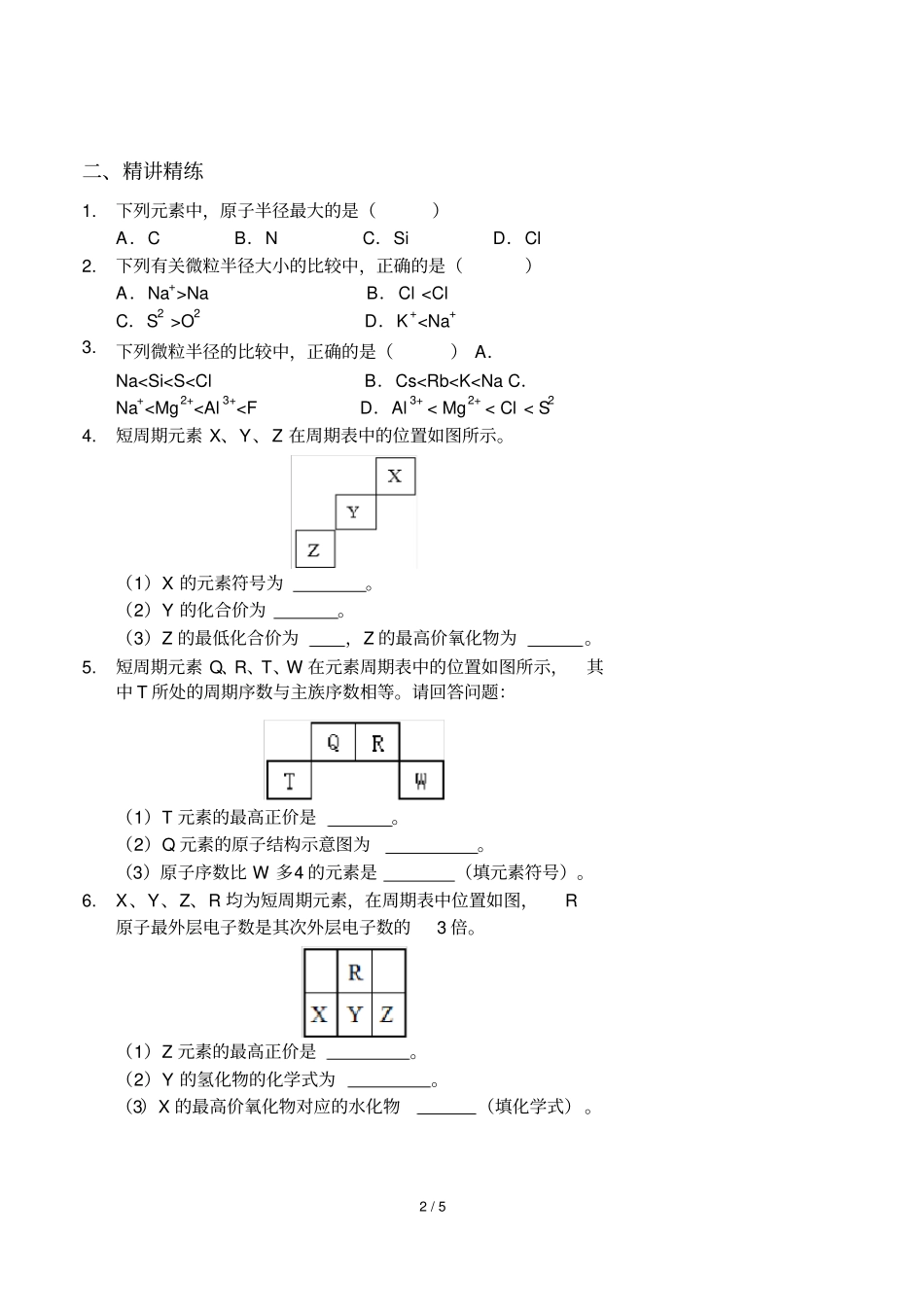
下列元素中,原子半径最大的是()A.CB.NC.SiD.Cl2
下列有关微粒半径大小的比较中,正确的是()A.Na+>NaB.ClO2D.K+X>ZB.X>Y>ZC.Y>Z>XD.Z>Y>X4/513
已知X、Y、Z元素的原子的电子层数相同,且其最高价氧化物对应水化物的酸性依次增强,下列判断正确的是()A.最高化合价按X、Y、Z的顺序减小B.单质的氧化性按X、Y、Z的顺序增