乾县二中化学必修二导学案班级:姓名元素周期表和元素周期律的应用导学案乾县二中李强【复习巩固】(1)同周期元素:同周期,电子层数相同,即原子序数越大,原子半径越,核对电子的引力越,原子失电子能力越,得电子能力越,金属性越、非金属性越
(2)同主族元素:同主族,电子层数越多原子半径越,核对电子引力越,原子失电子能力,得电子能力,金属性越、非金属性越
【基础知识】1
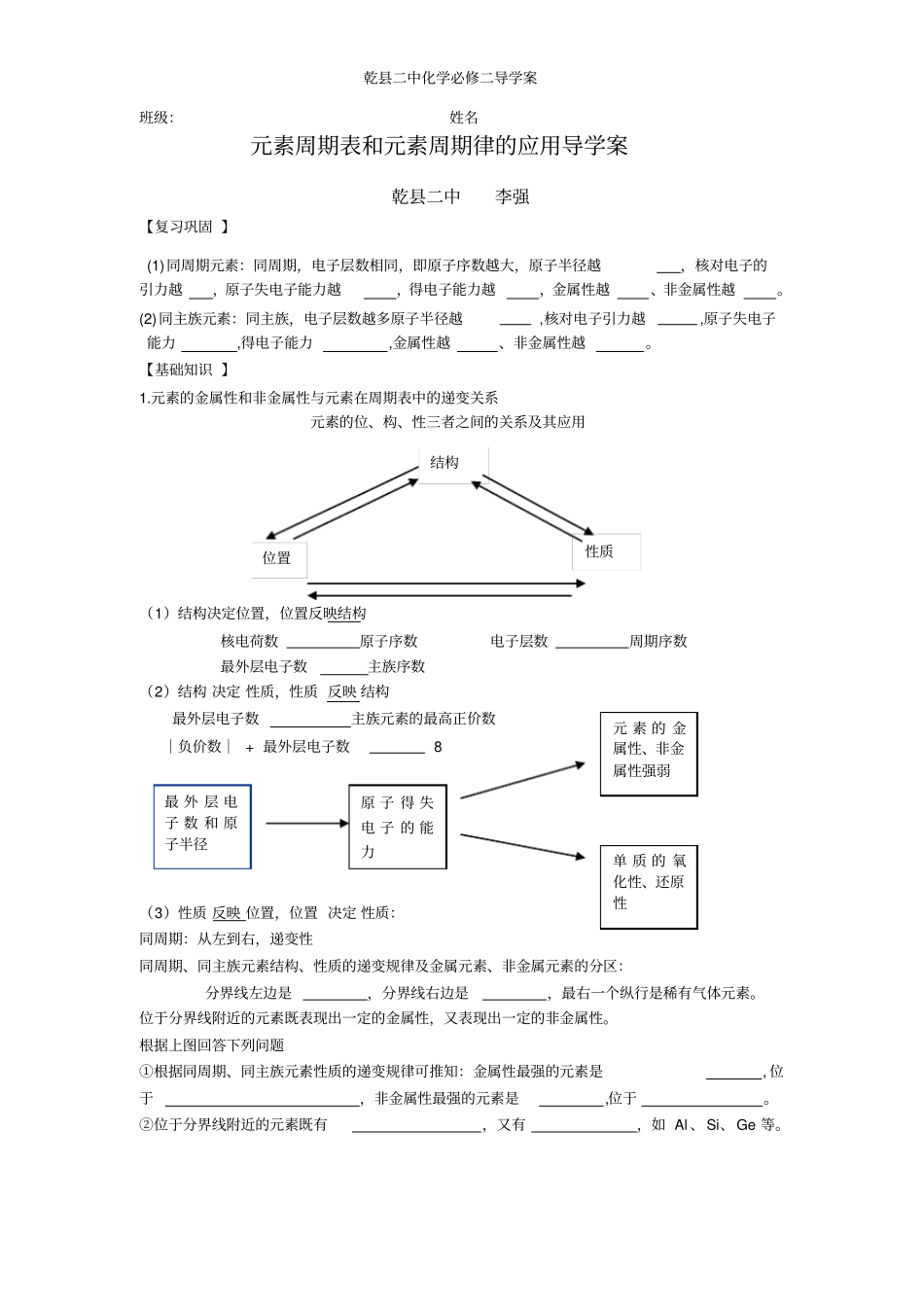
元素的金属性和非金属性与元素在周期表中的递变关系元素的位、构、性三者之间的关系及其应用(1)结构决定位置,位置反映结构核电荷数原子序数电子层数周期序数最外层电子数主族序数(2)结构决定性质,性质反映结构最外层电子数主族元素的最高正价数︱负价数︱+最外层电子数8(3)性质反映位置,位置决定性质:同周期:从左到右,递变性同周期、同主族元素结构、性质的递变规律及金属元素、非金属元素的分区:分界线左边是,分界线右边是,最右一个纵行是稀有气体元素
位于分界线附近的元素既表现出一定的金属性,又表现出一定的非金属性
根据上图回答下列问题①根据同周期、同主族元素性质的递变规律可推知:金属性最强的元素是,位于,非金属性最强的元素是,位于
②位于分界线附近的元素既有,又有,如Al、Si、Ge等
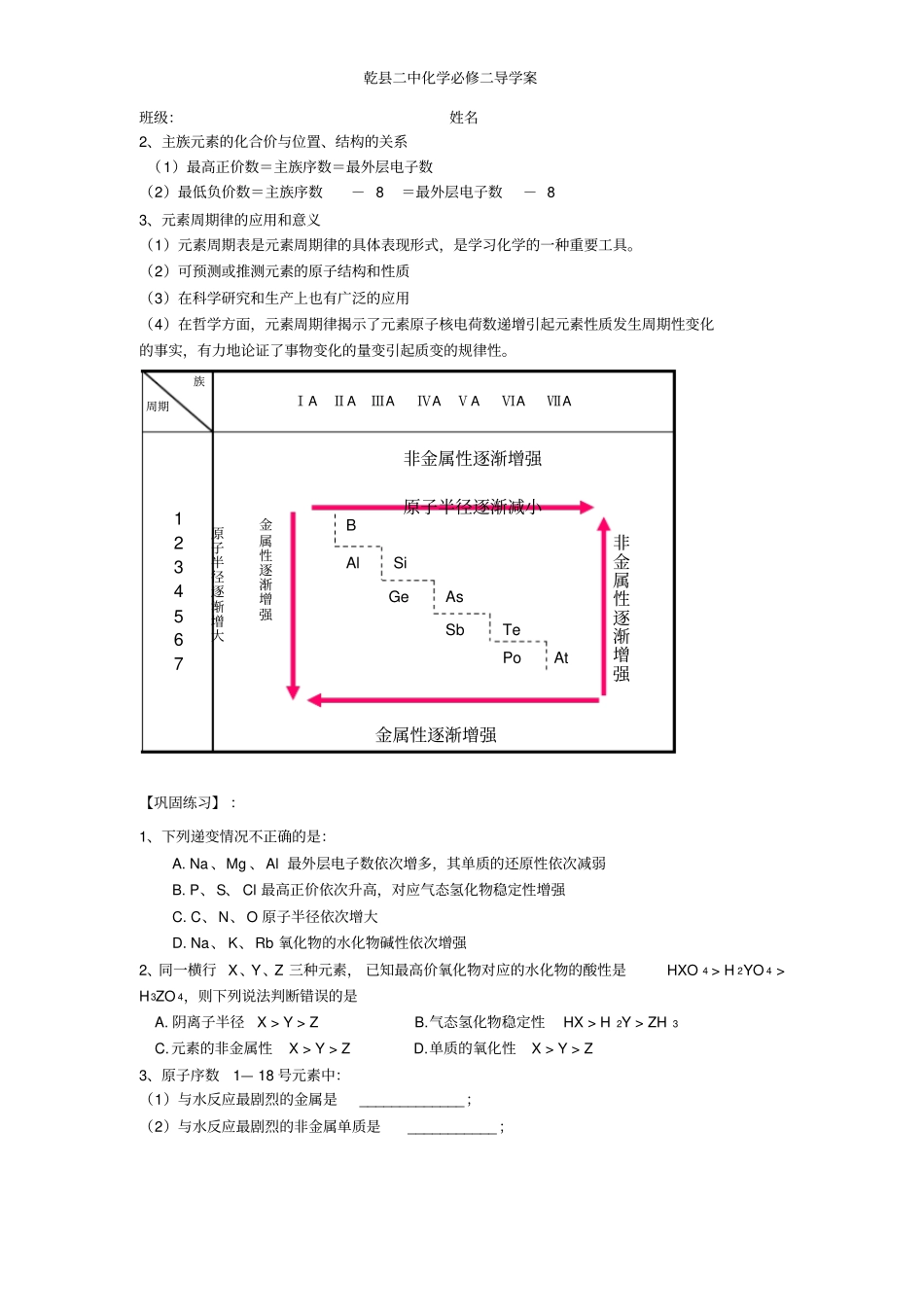
结构位置性质最外层电子数和原子半径元素的金属性、非金属性强弱原子得失电子的能力单质的氧化性、还原性乾县二中化学必修二导学案班级:姓名2、主族元素的化合价与位置、结构的关系(1)最高正价数=主族序数=最外层电子数(2)最低负价数=主族序数-8=最外层电子数-83、元素周期律的应用和意义(1)元素周期表是元素周期律的具体表现形式,是学习化学的一种重要工具
(2)可预测或推测元素的原子结构和性质(3)在科学研究和生产上也有广泛的应用(4)在哲学方面,元素周期律揭示了元素原子核电荷数递增引起元素性质发生周期性变化的事实,有力地论证了事物变化的量变引起质变