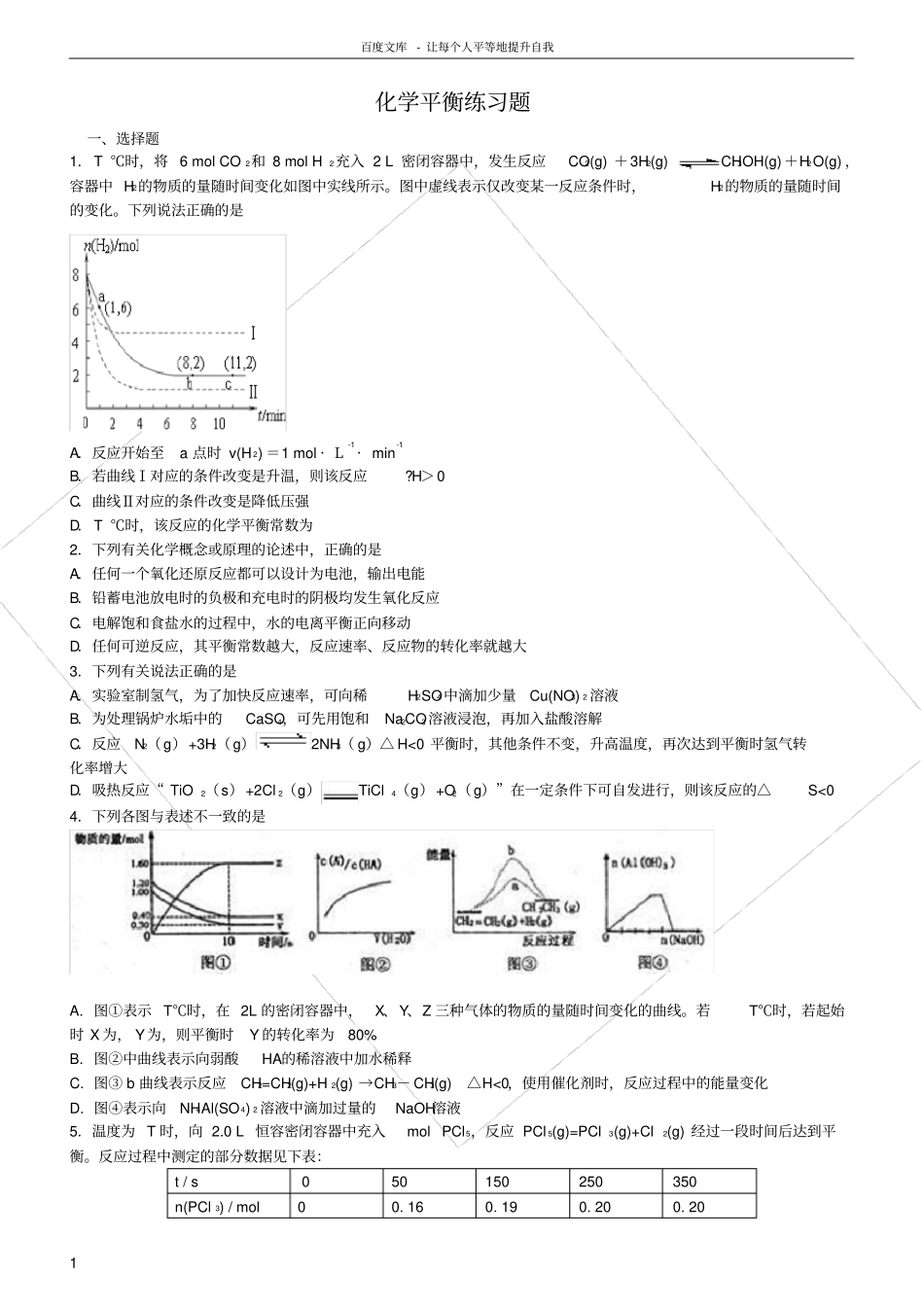
百度文库- 让每个人平等地提升自我1 化学平衡练习题一、选择题1.T ℃时,将 6 mol CO 2和 8 mol H2充入 2 L 密闭容器中,发生反应CO2(g) +3H2(g) CH3OH(g)+H2O(g) ,容器中 H2的物质的量随时间变化如图中实线所示
图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化
下列说法正确的是A.反应开始至a 点时 v(H 2) =1 mol · L-1· min-1B.若曲线Ⅰ对应的条件改变是升温,则该反应
H>0C.曲线Ⅱ对应的条件改变是降低压强D.T ℃时,该反应的化学平衡常数为2.下列有关化学概念或原理的论述中,正确的是A.任何一个氧化还原反应都可以设计为电池,输出电能B.铅蓄电池放电时的负极和充电时的阴极均发生氧化反应C.电解饱和食盐水的过程中,水的电离平衡正向移动D.任何可逆反应,其平衡常数越大,反应速率、反应物的转化率就越大3.下列有关说法正确的是A.实验室制氢气,为了加快反应速率,可向稀H2SO4 中滴加少量Cu(NO3) 2 溶液B.为处理锅炉水垢中的CaSO4,可先用饱和Na2CO3 溶液浸泡,再加入盐酸溶解C.反应N2(g)+3H2(g)2NH3( g)△ H