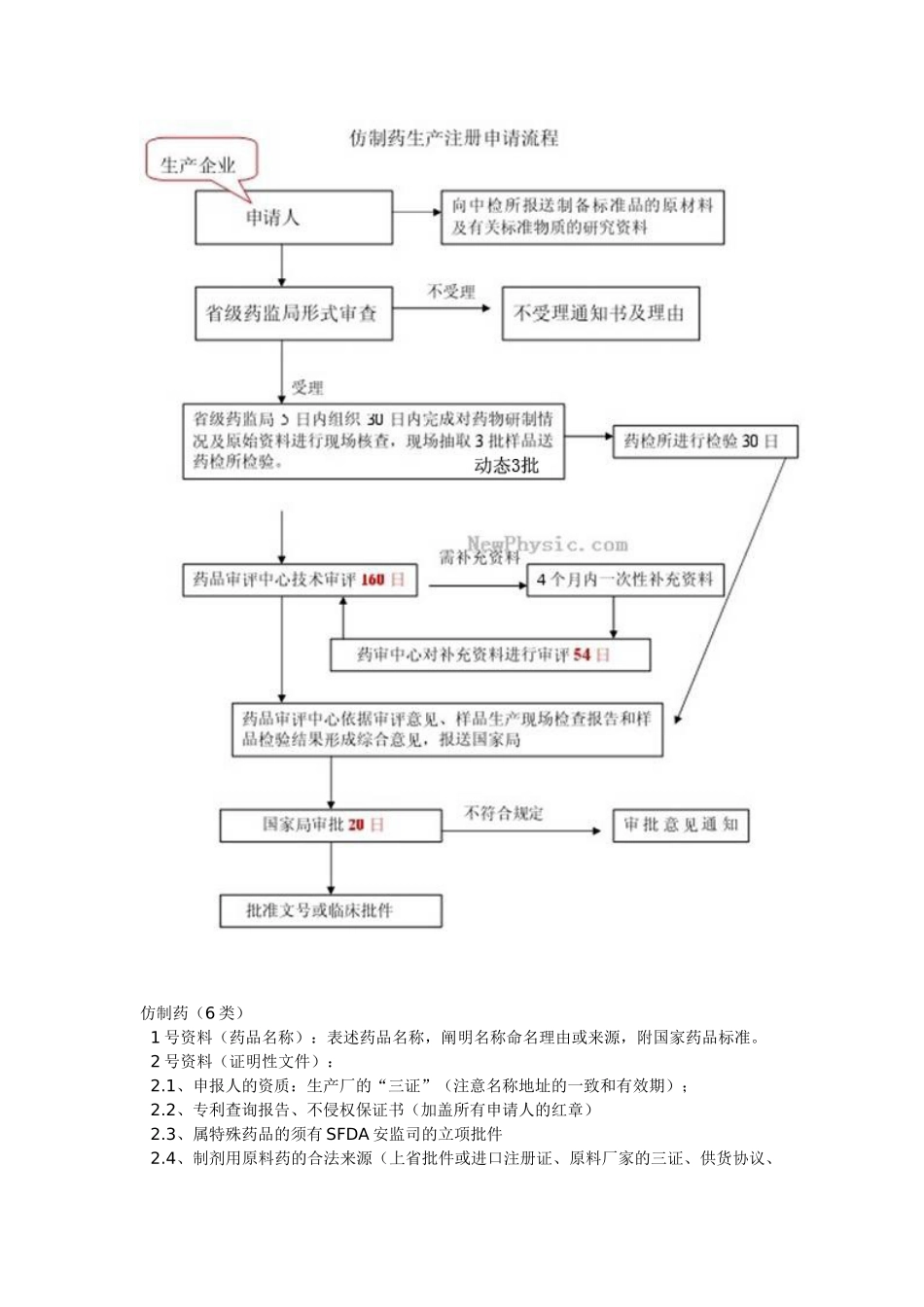
仿制药(6 类) 1 号资料(药品名称):表述药品名称,阐明名称命名理由或来源,附国家药品标准。 2 号资料(证明性文件): 2.1、申报人的资质:生产厂的“三证”(注意名称地址的一致和有效期); 2.2、专利查询报告、不侵权保证书(加盖所有申请人的红章) 2.3、属特殊药品的须有 SFDA 安监司的立项批件 2.4、制剂用原料药的合法来源(上省批件或进口注册证、原料厂家的三证、供货协议、购买发票、质量标准、出厂报告书及自检报告书),向经销单位购买的,还需提供经销商与原料厂的供货协议; 2.5、申请人同时申报原料与制剂的则不提供“2.4”的资料,若同时申请原料和制剂的厂家不是同一家,则须提供原料厂与制剂厂之间的供货协议或合作开发协议以及原料药受理单。(相同制剂,原料药只能和一个申请人合作申报)。 2.6、直接接触药品的包装材料或容器的供应商资质、包材注册证、报告书、质量标准 2.7、对照样品的购买发票、质量标准及检验报告书 2.8、委托试验:应提供委托合同,并附该机构合法登记证明、必要的资质证明。 2.9、新开办企业、新建车间或新增剂型的,在《生产许可证》上载明相应事项的后,方可申报生产 3 号资料(立题目的与依据): 参考药审中心的指导原则要求 4 号资料(对主要研究结果的总结及评价):参考药审中心的指导原则要求 5 号资料(药品说明书、起草说明及相关参考文献):格式符合 24 号令要求,贮藏条件与稳定性考察结果是否符合,提供被仿产品的最新的说明书复印件。 6 号资料(包装、标签设计样稿):内容符合 24 号令要求 7 号资料(药学研究资料综述):参考药审中心的指导原则要求 8 号资料(原料药生产工艺的研究资料及文献资料;制剂处方及工艺的研究资料及文献资料):参考现场检查要求,申报时要确定规模化生产工艺、质控要点及工艺验证 9 号资料(确证化学结构或者组份的试验资料及文献资料):不提交 10 号资料(质量研究工作的试验资料及文献资料):参考药审中心的指导原则要求 11 号资料(药品标准及起草说明):参考国家标准,不能低于现有标准,附上国家标准等参考标准 12 号资料(样品的检验报告书):中试规模以上申报样品的自检报告书(3 批),完成生物等效试验后还应附上药检所检验的三批报告书复印件 13 号资料(原料药、辅料的来源及质量标准、检验报告书): 原料合法来源证明文件一套(同 2 号资料中的原料资质)辅料的来源(厂家三证、...