第九单元 溶液课题 1 溶液的形成1
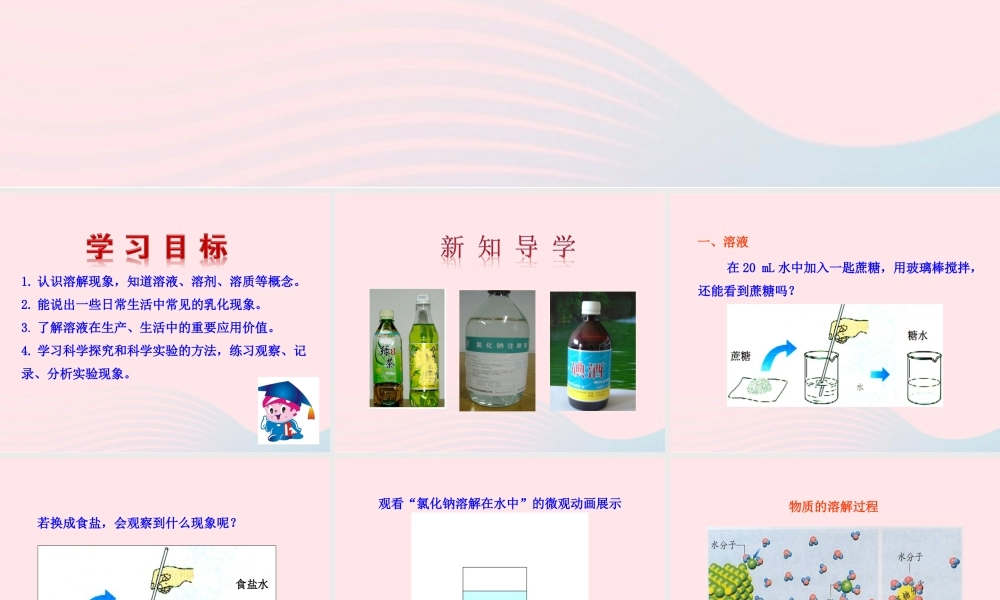
认识溶解现象,知道溶液、溶剂、溶质等概念
能说出一些日常生活中常见的乳化现象
了解溶液在生产、生活中的重要应用价值
学习科学探究和科学实验的方法,练习观察、记录、分析实验现象
在 20 mL 水中加入一匙蔗糖,用玻璃棒搅拌,还能看到蔗糖吗
一、溶液若换成食盐,会观察到什么现象呢
食盐20 mL 水食盐水观看“氯化钠溶解在水中”的微观动画展示物质的溶解过程蔗糖溶解与氯化钠溶解的比较形成什么微观解释存在的微粒蔗糖溶解氯化钠溶解蔗糖溶液蔗糖分子扩散到水分子间蔗糖分子、水分子氯离子和钠离子分散在水分子间氯化钠溶液氯离子、钠离子、水分子结论:食盐溶于水后,形成了自由移动的离子,因此可以导电;蔗糖溶于水后仍然以分子形式存在,因此不能导电
溶液:溶剂:溶质: 一种或几种物质分散到另一种物质里,形 成均一的、稳定的混合物 , 叫做溶液
能溶解其他物质的物质被溶解的物质溶 液溶 质溶 剂医用酒精硝酸钾溶液硫酸铜溶液汽 水稀硫酸碘 酒石灰水氢氧化钙 Ca(OH)2H2O硫酸铜 CuSO4硝酸钾 KNO3酒精 C2H5OHCO2 等碘 I2硫酸 H2SO4酒精 C2H5OHH2OH2OH2OH2OH2O指出下列常见溶液中的溶质和溶剂
水是一种最常见的溶剂,汽油等也是常见的溶剂;3
不同溶质在同种溶剂中,溶解能力也不同
同种溶质在不同溶剂中,溶解能力不同;溶剂溶质结论结论水水乙醇水和乙醇能够互溶 物质在溶解时,常常会使溶液的温度发生改变,这说明物质在溶解的过程中通常伴随着热量的变化:有的物质在溶解时会出现吸热的现象,有的物质在溶解时会出现放热的现象
溶质不同,这两种过程吸收或放出热量不同,从而使溶液的温度发生不同的变化
二、溶解时的吸热或放热现象NaClNH4NO3NaOH溶解前后温度的变化不变降低升高猜猜猜猜