浓 盐 酸溴水20 四川省成都市 2016-2017 学年高二化学下学期半期考试试题考试时间: 90 分钟总分: 100 分原子量: Li — 7 Al— 27 S— 32 O— 16 Mg— 24 Cu— 64 Zn— 65 Pb— 207 第 Ⅰ卷选 择 题 (共40 分 )一、选择题(每小题只有一个选项符合题意,每小题 2 分,共 40 分) 1 .下列化学用语使用正确的组合是 ( ) ①丙烯的结构简式为CH3CHCH2 ②乙炔分子的比例模型③有机还原剂 LiAlH 4 中,氢显- 1 价④质量数为 40 的钙原子: 40Ca⑤NH4Cl 的电子式:⑥2
甲基 -1- 丁醇的结构简式:A.①④B.③④C.④⑤D.⑤⑥2
下列有关说法正确的是( ) A.在海轮外壳镶嵌铜块,能减缓轮船的腐蚀,是利用牺牲阳极的阴极保护法B.其他条件相同时, 增大反应物浓度使反应物中活化分子百分比增大,从而反应速率增大
C.酸碱指示剂是一些有机弱酸或弱碱,在溶液中存在电离平衡,勒夏特列理论可以解释酸碱指示剂的指示原理D.Fe2+可用蓝色的 K3[Fe(CN) 6] 溶液进行检验3
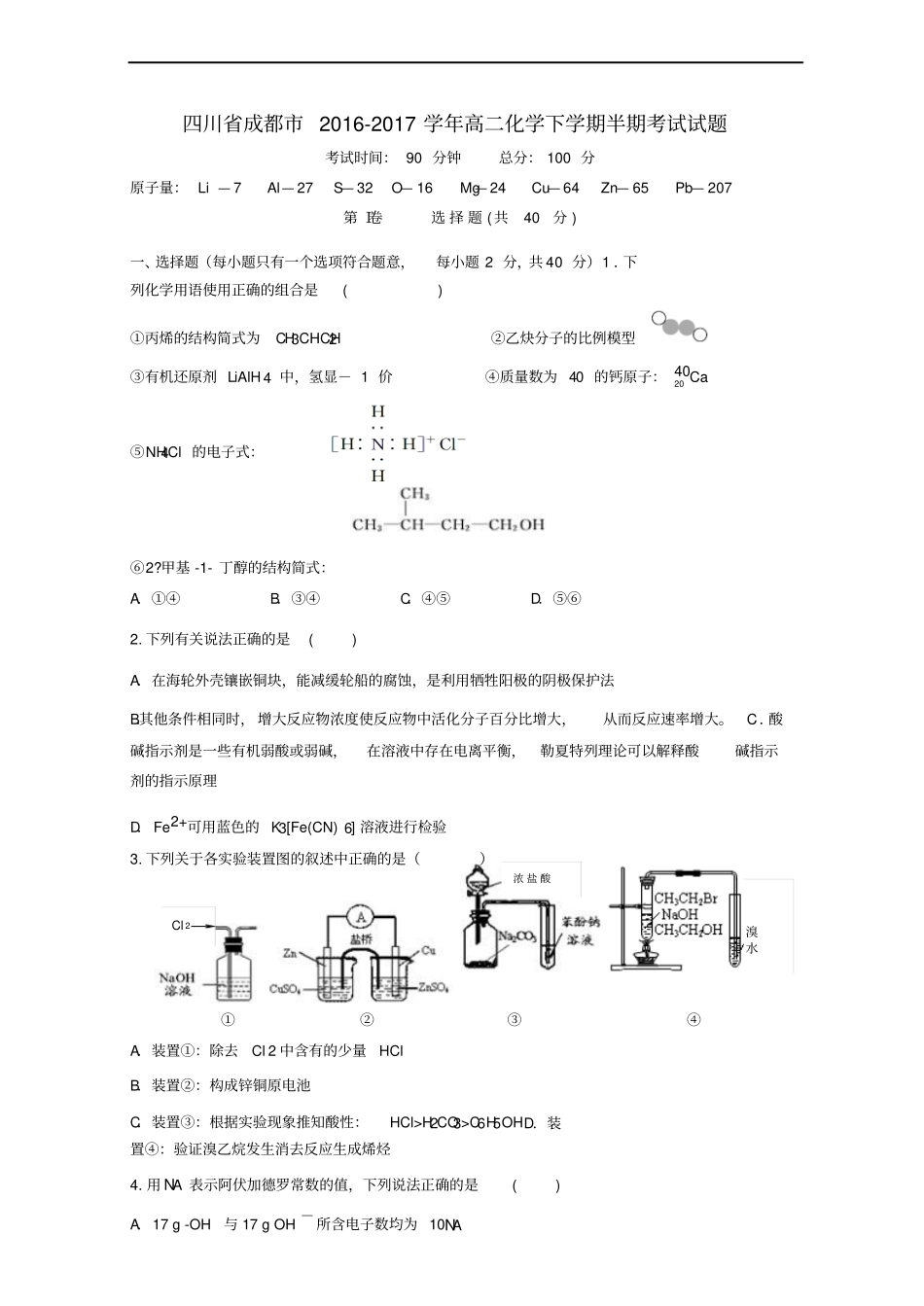
下列关于各实验装置图的叙述中正确的是()①②③④A.装置①:除去Cl 2 中含有的少量HCl B.装置②:构成锌铜原电池C.装置③:根据实验现象推知酸性:HCl>H2CO3>C6H5OH D.装置④:验证溴乙烷发生消去反应生成烯烃4
用 NA 表示阿伏加德罗常数的值,下列说法正确的是( ) A.17 g -OH 与 17 g OH -所含电子数均为 10NACl 2 2B.标准状况下, 11
2 L 的甲醇所含的氢原子数等于2NA 3C.在铅蓄电池放电时,正极增重32g,转移的电子数为NA D.1 mol 苯酚分子中含有的碳碳双键数为3NA 5
下列热化学方程式书写正确的是()A.甲烷的燃烧热为890 k