复分解反应的条件复分解反应的条件复分解反应A+ C=BABDCD+复分解反应要发生,且能够进行到底,一般应考虑两方面的条件:1 、考虑反应发生的基本条件(对反应物要求的条件)2 、对生成物的条件要求 两者缺一不可问题的提出:复分解反应包括: 酸 + 碱——盐 + 水 酸 + 盐——新酸 + 新盐 碱 + 盐——新碱 + 新盐 盐 + 盐——新盐 + 新盐 酸 + 金属氧化物——盐 +水那么酸碱盐之间一定能发生复分解反应吗
类型一:酸 + 碱——盐 +水HCl NaOH+HCl NaOH=+H2OH2SO4+Cu(OH)2=H SO4 Cu OHHOH+2H2O酸 + 碱——盐 +水条件:( 1 )酸和碱至少有一种可溶;( 2 )若酸是常见的三种强酸,无论碱 是否可溶,反应均可以进行
三大强酸:盐酸、硫酸、硝酸酸、碱的溶解规律酸:初中范围内的酸全溶碱:钾、钠、钡、铵,四碱 溶, Ca(OH)2 微溶, 其余的全不溶
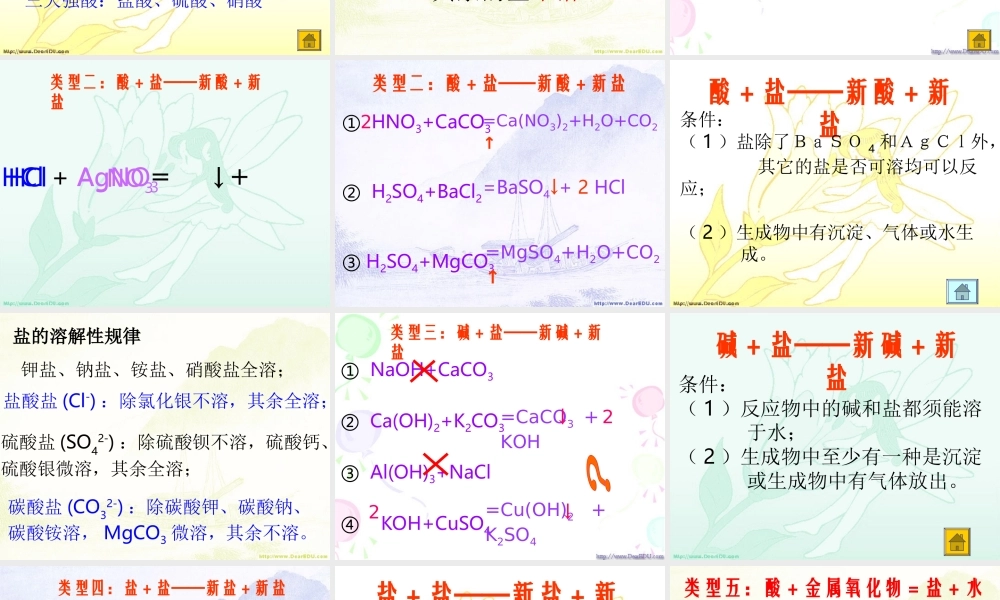
酸和碱反应的其他例子① HNO3+ Fe(OH)3② HCl +Ca(OH)2 =Fe(NO3)3+ H2O33= CaCl2 + H2O22类型二:酸 + 盐——新酸 + 新盐HCl + AgNO3HClNO3Ag=↓ +类型二:酸 + 盐——新酸 + 新盐① HNO3+CaCO3② H2SO4+BaCl2③ H2SO4+MgCO3=Ca(NO3)2+H2O+CO2↑2=BaSO4↓+ 2 HCl=MgSO4+H2O+CO2↑酸 + 盐——新酸 + 新盐条件:( 1 )盐除了BaSO 4 和AgCl外, 其它的盐是否可溶均可以反应;( 2 )生成物中有沉淀、气体或水生 成
盐的溶解性规律钾盐、钠盐、铵盐、硝酸盐全溶;盐酸盐 (Cl-) :除氯化银不溶,其余全溶;硫酸盐 (SO42-) :除硫酸钡不溶,硫酸钙、硫酸银微溶,其余全溶;碳酸盐 (CO32-) :除