2017-2018学年度怀柔区零模试化学试题可能用到的相对原子质量:C12H1O166
“化学使生活更美好
”,能充分体现这句话的是:A
磁悬浮列车的使用,使交通更迅捷B
杂交水稻的推广,使中国走上富裕之路C
青蒿素的研制成功,为疟疾患者带来福音D
扫描隧道显微镜的使用,使人们观察到微观世界的美好7
饮茶是中国人的传统饮食文化之一
为方便饮用,可通过以下方法制取罐装饮料茶:上述过程涉及的实验方法、实验操作和物质作用说法不正确的是A
①操作利用了物质的溶解性B
③操作为分液C
②操作为过滤D
加入抗氧化剂是为了延长饮料茶的保质期8
短周期元素X、Y、Z、W在周期表中的位置关系如图
下列说法一定不正确的是A
Z原子比X原子的最外层电子数多2个B
原子半径:W>X>Z>YC
最高价氧化物对应的水化物的碱性:X>WD
Y单质与氢气反应条件比Z单质更苛刻9
在右图所示实验装置中,向盛有溶液①和溶液②的试管中,通入过量气体X,最终溶液①、溶液②均无沉淀生成的是:1O
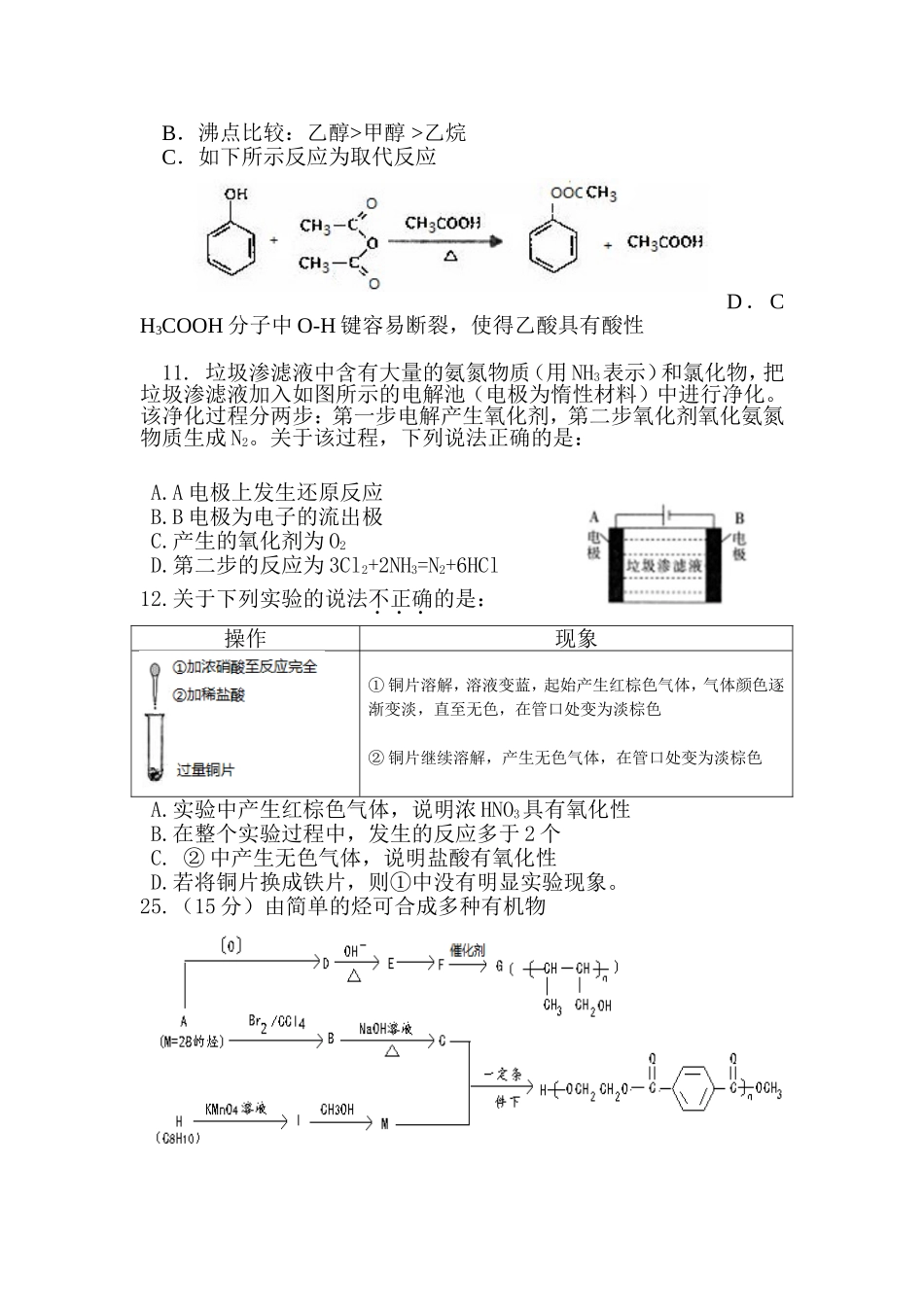
下列关于有机化合物的叙述不正确的是A.等物质的量的A、B两种烃分别完全燃烧后,生成的CO2与消耗的O2的物质的量均相同,则A和B一定互为同系物选项气体X溶液①溶液②ASO2Ca(OH)2BaCl2BCl2AgNO3Na2SCNH3AgNO3AlCl3DHClNa2SiO3NaAlO2B.沸点比较:乙醇>甲醇>乙烷C.如下所示反应为取代反应D.CH3COOH分子中O-H键容易断裂,使得乙酸具有酸性11
垃圾渗滤液中含有大量的氨氮物质(用NH3表示)和氯化物,把垃圾渗滤液加入如图所示的电解池(电极为惰性材料)中进行净化
该净化过程分两步:第一步电解产生氧化剂,第二步氧化剂氧化氨氮物质生成N2
关于该过程,下列说法正确的是:A
A电极上发生还原反应B
B电极为电子的流出极C
产生的氧化剂为O2D
第二步的反应为3Cl2+2NH3