利用化学方程式的简单计算 学习目标1 、在理解化学方程式涵义的基础上,掌握有关反应物、生成物质量的计算
2 、通过有关化学方程式计算,掌握化学方程式计算的书写格式,同时培养、提高思维能力和解题能力
学习重点1 、掌握已知一种反应物(或生成物)的质量,求生成物(或反应物)的质量
2 、根据化学方程式计算的书写格式规范化
复习提问以镁在空气中燃烧为例说明化学方程式的涵义
镁在空气中燃烧反应中反应物与生成物之间的质量比可表示为:2Mg + O2 ====== 2 Mg O 2×24 : 16×2 : ( 24+16 ) ×2 48 : 32 : 80若: 48 克 : ( )克 : ( ) 克点燃若:( )克 : ( )克 : 4 0 克 说明:在化学反应中,反应物与生成物之间的质量比是成正比例关系
因此,利用正比例关系根据化学方程式和已知的一种反应(或生成物)的质量,可求生成物(反应物)
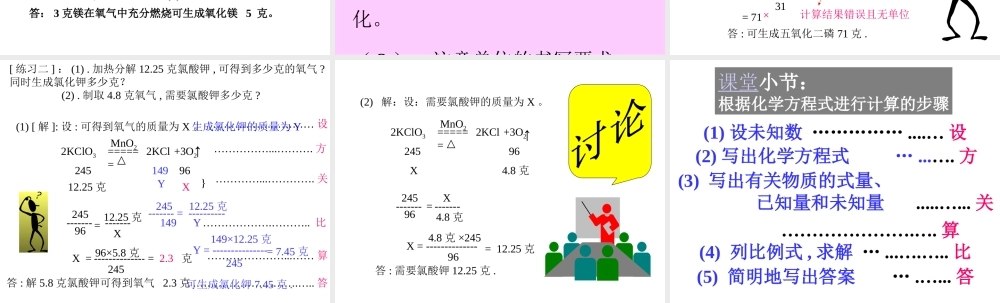
[ 例题 ] : 3 克镁在氧气中充分燃烧,可以生成多少克氧化镁
解:设可生成氧化镁的质量为 X(1) 设未知数 …
设2 Mg + O 2 ====== 2 Mg O点燃48 803 克 X (2) 写出化学方程式…
方} (3) 写出有关物质的式量、 已知量和未知量
关48------ = ------803 克X(4) 列比例式 , 求解
比X = ------------ 80×3 克48= 5 克答: 3 克镁在氧气中充分燃烧可生成氧化镁 5 克
……………………………
算 (5) 简明地写出答案…
答 根据化学方程式计算的注意事项 :( 1 )
根据物质的组成求各化学式的式量与化学式前边系数的乘积之比,计算时必须准确无误
解题格式的书写要规范化