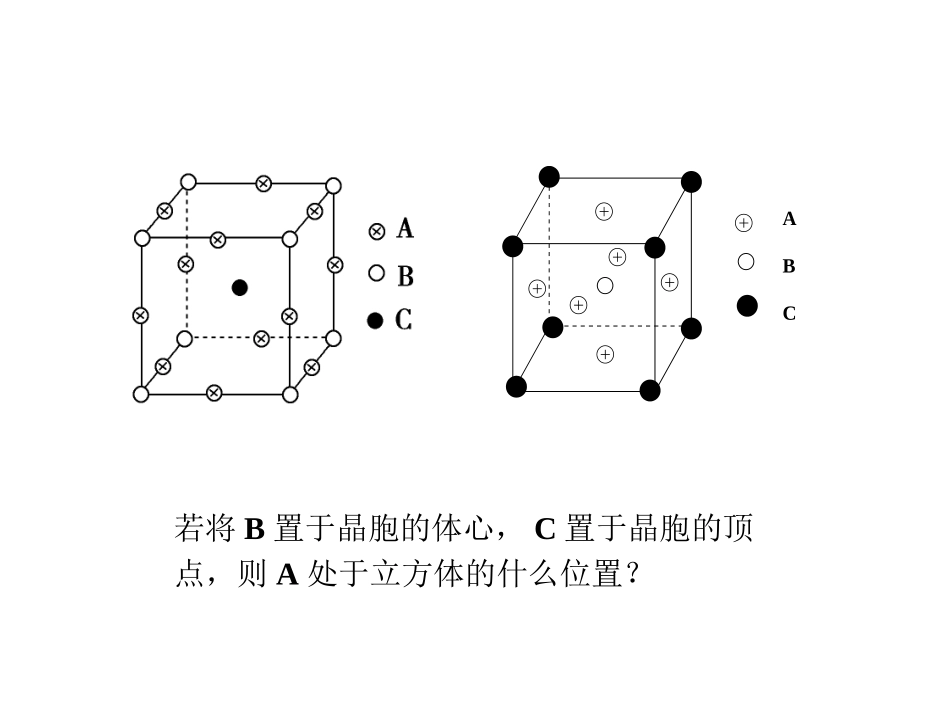
研讨上图为KIO3晶胞结构,在另一种表示中,I处于各顶角位置,则K处于________位置,O处于________位置
研讨若将B置于晶胞的体心,C置于晶胞的顶点,则A处于立方体的什么位置
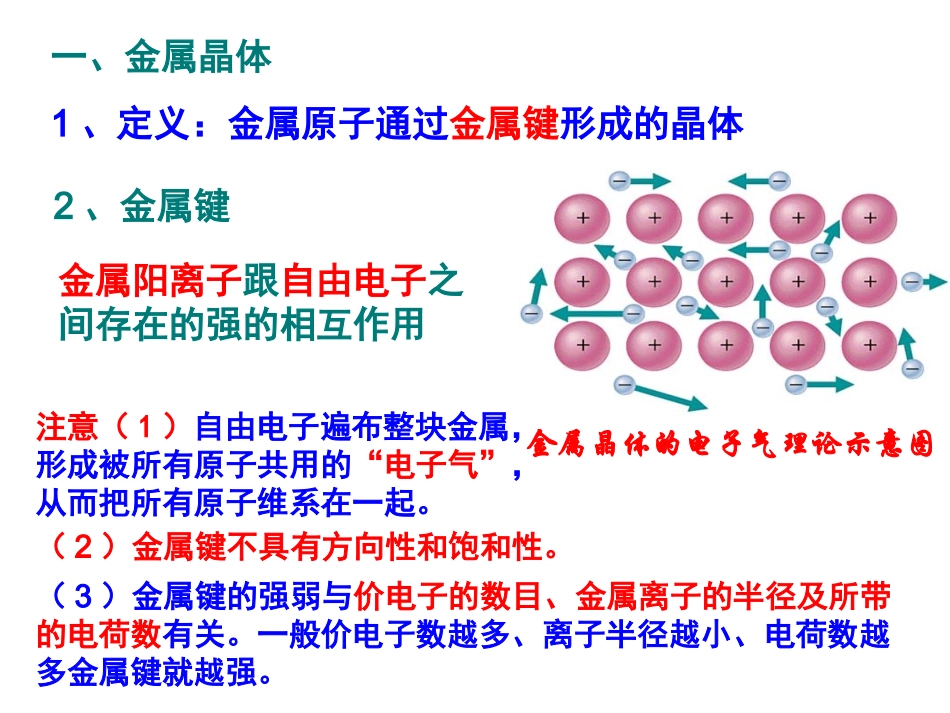
ABC一、金属晶体1、定义:金属原子通过金属键形成的晶体2、金属键金属阳离子跟自由电子之间存在的强的相互作用金属晶体的电子气理论示意图(2)金属键不具有方向性和饱和性
注意(1)自由电子遍布整块金属,形成被所有原子共用的“电子气”,从而把所有原子维系在一起
(3)金属键的强弱与价电子的数目、金属离子的半径及所带的电荷数有关
一般价电子数越多、离子半径越小、电荷数越多金属键就越强
思考:1、如何解释金属存在的金属光泽、延展性、导电性和导热性等共同的物理性质
(见课本P56、79)2、合金一般都具有硬度大、熔点低的特点,为什么
(见课本P79-80)3、金属晶体的原子堆积模型(1)简单立方堆积相邻非密置层原子的原子核在同一条直线上,原子的配位数为6,每个晶胞含1个原子,空间利用率为52%(
)代表物质:钋(Po)(2)钾型(体心立方堆积-A2)原子的配位数为8,每个晶胞含2个原子,空间利用率为68%
代表物质:碱金属Fe等(3)镁型(六方最密堆积-A3)原子的配位数为12,每个晶胞含2个原子,空间利用率为74%
代表物质:MgZnTi(4)铜型(面心立方堆积-A1)原子的配位数为12,每个晶胞含4个原子,空间利用率为74%
代表物质:CuAgAu二、离子晶体1、定义:由阳离子和阴离子通过离子键结合而成的晶体
成键粒子:阴、阳离子相互作用力:离子键常见的离子晶体:强碱、活泼金属氧化物、大部分的盐类
(1)钠离子和氯离子的位置:钠离子:体心和棱心;氯离子:面心和顶点,或者反之
2、晶胞类型(1)氯化钠型晶胞(2)每个晶胞含钠离子、氯离子的个数(3)与Na+等距离且最近的Na+、Cl-各有几个