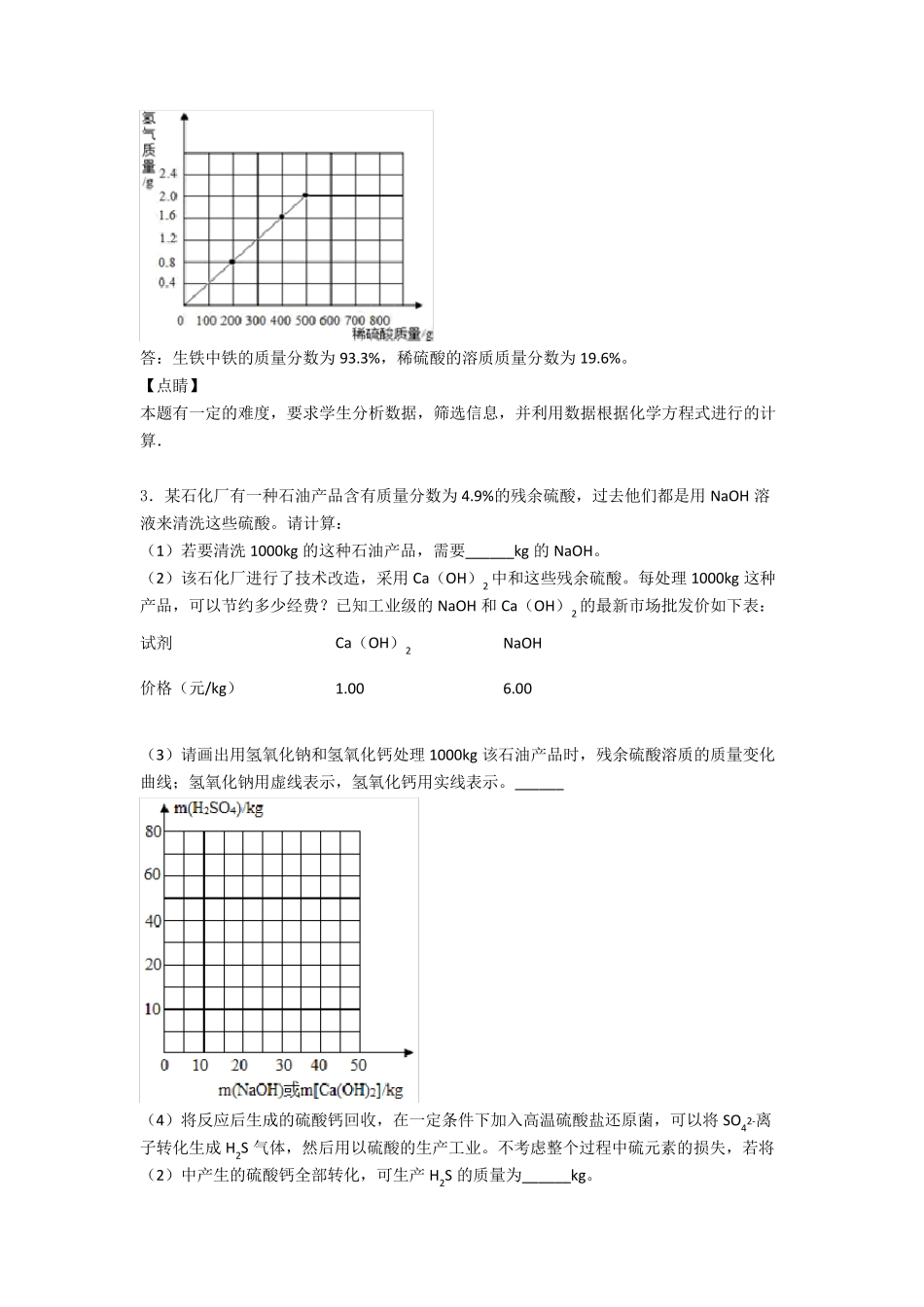
中考化学计算题汇编经典 一、中考化学计算题 1.取一定量的木炭在氧气中燃烧,生成23.2 g 气体(氧气已完全反应)。将气体通入过量的澄清石灰水中,生成40 g 沉淀。 计算: (1)生成气体的成分及质量___________。 (2)生成气体中碳元素的质量分数_________。 【答案】CO、CO2 的混合气体,其中CO 为5.6g,CO2 为17.6g 31% 【解析】 【详解】 (1)设生成二氧化碳的质量为x 2232Ca(OH) +CO =CaCO+H O44100x40g 44100=x40g , x=17.6g CO 的质量=23.2g-17.6g=5.6g; (2)生成气体中碳元素的质量分数= (17.6g× 12100%44 +5.6g× 1228 ×100%)÷23.2 g ≈31%;答:此气体为CO、CO2 混合气体,其中CO 为5.6g,CO217.6g;气体中碳元素的质量分数为31%。 2.某化学兴趣小组为了分析生铁中铁的含量,进行了实验研究,即取60g 经粉碎后的生铁,把 800 稀硫酸分4 次加入到该样品中,测得数据记录如下表: 第 1 次 第 2 次 第 3 次 第 4 次 加入稀硫酸质量(g) 200 200 200 200 剩余固体质量(g) 37.6 15.2 4 4 (说明:生铁中杂质不溶于水,也不与硫酸反应.) (1)第 2 次测得剩余固体质量为15.2g,其成分为_____. A 铁 B 铁和碳 C 碳 (2)生铁中铁的质量分数为多少?(写出计算过程,结果保留到小数点后一位)_____ (3)计算所用稀硫酸的溶质质量分数为多少?_____(写出计算过程,结果保留到小数点后一位)并画出反应生成的氢气质量与加入稀硫酸质量的关系图._____ 【答案】B 93.3% 19.6% 【解析】 【详解】 (1)分析图表可发现向第二次的剩余固体中加硫酸,固体继续减少,说明第二次剩余固体中铁剩余,当然碳不反应,也剩余.故答案为:B (2)表中第3、第4 次剩余固体都是 4g,可知最终剩余固体4g 为碳,所以生铁中铁的质量分数为:60g-4g100%=93.3%60g (3)从第1、第2 次中可得出结论:每 200g 硫酸可以完全反应37.6g﹣15.2g=22.4g 铁, 设 200g 稀硫酸中的溶质质量为x,22.4g 铁反应生成氢气的质量为y 则 2442=5698 Fe +H SOF222.eSO +H4gxy 5698222.4gxy 解之得:x=39.2g,y=0.8g 稀硫酸的溶质质量分数为:39.2g100%19.6%200g 可得出 56g 铁反应生成氢气的质量为 560.8g2g22.4,恰好反应消耗的硫酸质量为500g 由于铁和硫酸反应生成氢气的质量和反应的500g 硫酸成正比,所以图象如下: 答:生...