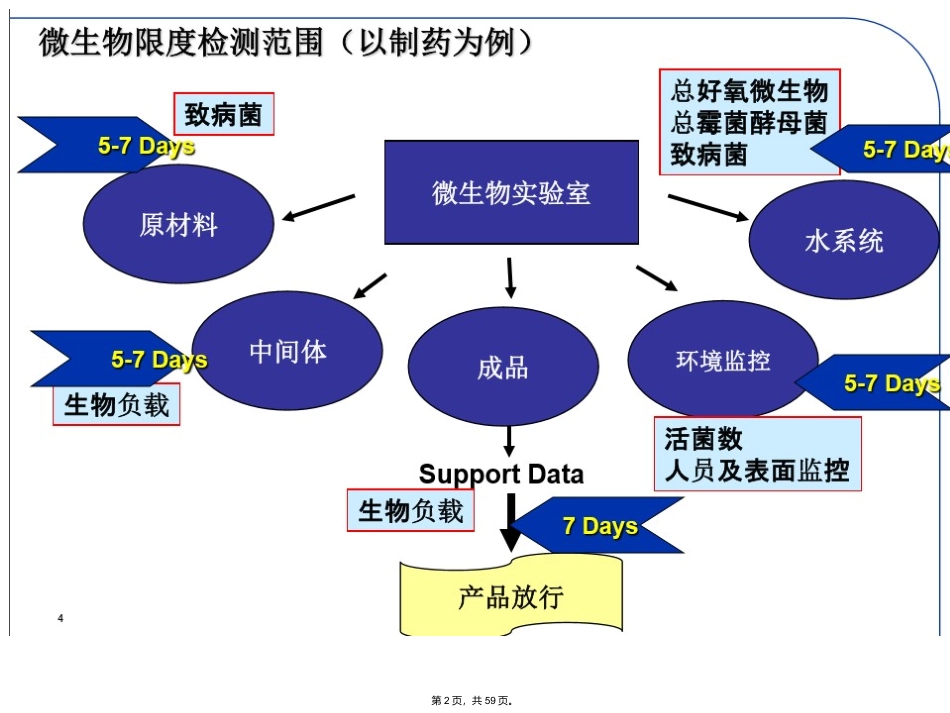
微生物限度检查法《中国药典》2015年版修订后将分为三个附录:–1、非无菌产品微生物限度检查:微生物计数法–2、非无菌产品微生物限度检查:控制菌检查法–3、非无菌药品微生物限度标准第1页,共59页
第2页,共59页
第3页,共59页
1总则:环境、要求1
2计数方法:平皿法、薄膜过滤法、最可能数法(MPN法)1
3计数培养基适用性检查和供试品计数方法适用性试验:菌种及菌液制备、培养基适用性检查、计数方法适用性试验
4供试品检查:检验量、供试品检查1
5结果判断1
6稀释液、冲洗液及培养基1
非无菌产品微生物限度检查:----微生物计数法第4页,共59页
•微生物计数法系用于能在有氧条件下生长的嗜温细菌和真菌的计数
•当本法用于检查非无菌制剂及其原、辅料等是否符合规定的微生物限度标准时,应按规定进行检验,包括样品的取样量和结果的判断等
除另有规定外,本法不适用于活菌制剂的检查
•本检查法可采用替代的微生物检查法,包括自动检测方法,但必须证明替代方法等效于药典规定的检查方法
1总则:第5页,共59页
1总则:•环境:–微生物计数试验环境应符合微生物限度检查的要求
(在不低于GMP现行版要求的D级洁净环境、局部洁净度不低于B级的单向流空气区域内进行)【10版:在环境洁净度10000级下的局部洁净度100级的单向流空气区域内】
–检验全过程必须严格遵守无菌操作,防止再污染,防止污染的措施不得影响供试品中微生物的检出
–单向流空气区域、工作台面及环境应定期进行监测
第6页,共59页
1总则:•如供试品有抗菌活性,应尽可能去除或中和
供试品检查时,若使用了中和剂或灭活剂,应确认其有效性及对微生物无毒性
•供试液制备时如果使用了表面活性剂,应确认其对微生物无毒性以及与所使用中和剂或灭活剂的相容性
第7页,共59页
•平皿法•薄膜过滤法•最可能数法(Most-Proba