初二科学 1 溶解度和质量分数的计算 【学习目标】 1
学会浓溶液稀释的计算
知道配制某一溶质的质量分数的溶液的方法和步骤
巩固对溶解度的涵义的理解
理解溶解度计算的基本思路
【知识要点】 一、配制溶质质量分数一定的溶液 1
用固体配制溶液: ①步骤: 计算、称量、溶解
②所用仪器:托盘天平、胶头滴管、量筒、药匙、烧杯、玻璃棒
例:配制溶液的质量分数为 10%的氯化钠溶液50g
步骤: (1)计算:溶质的质量:gg5%1 05 0;溶剂的质量:ggg4 555 0; 水的体积:mLmLgg4 5/14 5 (2)称量:用托盘天平称量5g氯化钠倒入烧杯中,用50mL量筒量取 45mL水倒入烧杯中
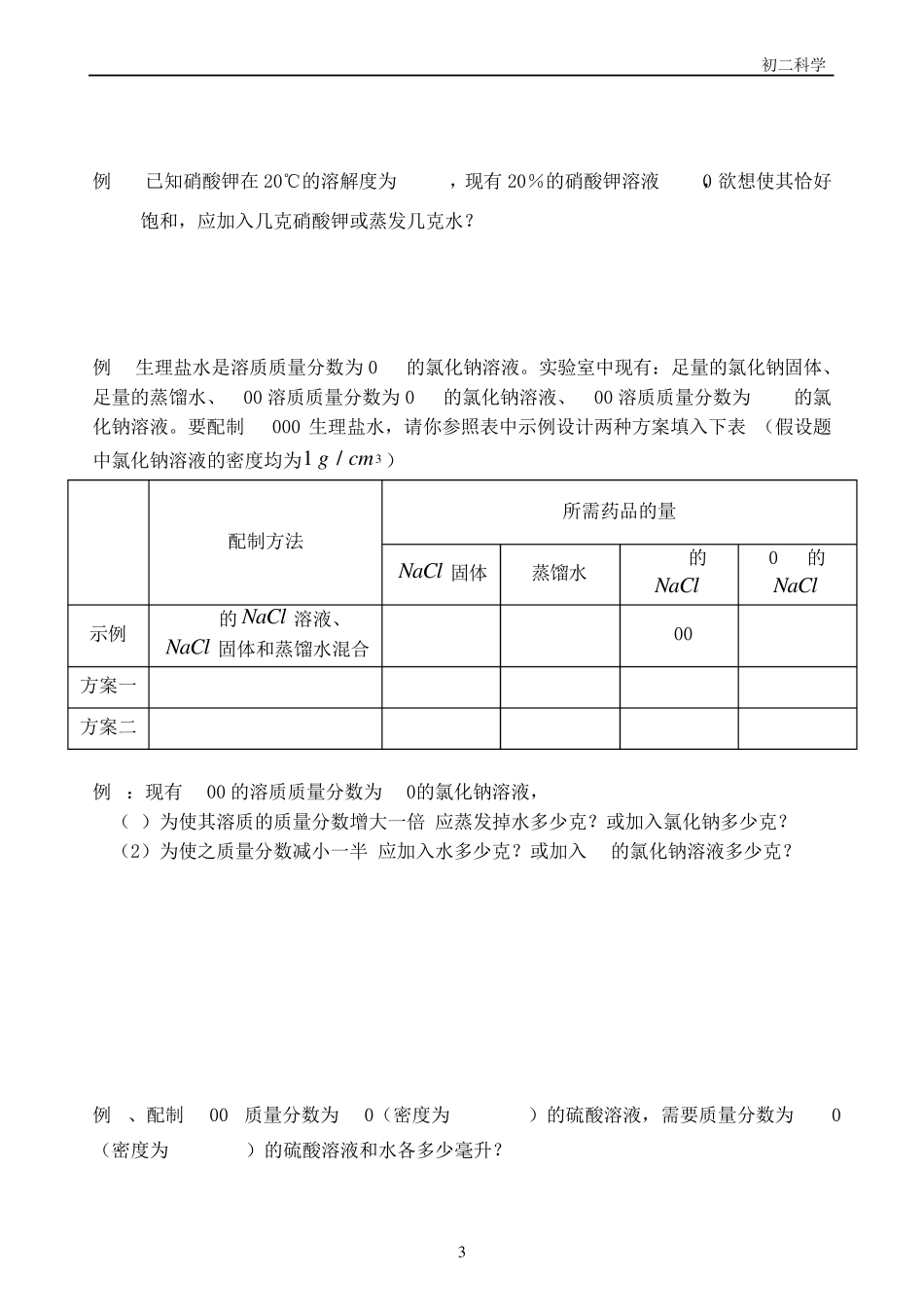
(3)溶解:用玻璃棒搅拌,加速固体物质的溶解速率,待氯化钠完全溶解得到的溶液即为 10%的氯化钠溶液50g
实验操作步骤如下图所示
用浓溶液配制稀溶液: ①步骤: 计算、量取、溶解
②所用仪器: 胶头滴管、量筒、烧杯、玻璃棒
二、有关溶液的计算依据 溶液浓缩方法:加入溶质,蒸发溶剂,加入高浓度的浓溶液
溶液稀释方法:加入溶剂,加入低浓度的稀溶液
1.加溶剂稀释和蒸发溶剂浓缩(没有晶体析出)的计算依据,变化前后溶液中溶质的质量相等,可用下列关系式表示:2211wmwm,已知三量通过方程可求另一量
2.加溶质增浓的计算:加入溶质溶解后,溶质和溶液质量都增加
增浓后的溶质质量分数=%1 0 0加入的溶液的质量原溶液质量加入的溶质质量原溶质质量
初二科学 2 3.两种浓度不同的同种溶质的溶液混合后,所得的溶液中溶质的质量分数一定大于小浓度,小于大浓度的溶质的质量分数
混合溶液中溶质的质量分数=%1002121的质量溶液的质量溶液中溶质质量溶液中溶质质量溶液 溶液中溶质质量=溶液质量×该溶液中溶质的质量分数