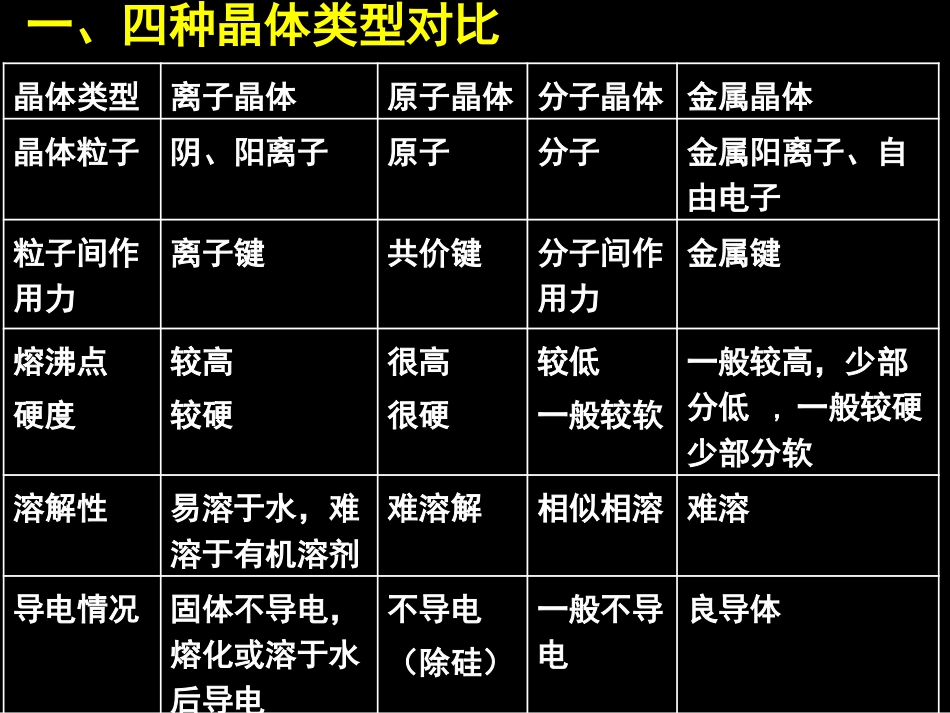
常见晶体类型主讲汪毅晶体类型离子晶体原子晶体分子晶体金属晶体晶体粒子阴、阳离子原子分子金属阳离子、自由电子粒子间作用力离子键共价键分子间作用力金属键熔沸点硬度较高较硬很高很硬较低一般较软一般较高,少部分低,一般较硬少部分软溶解性易溶于水,难溶于有机溶剂难溶解相似相溶难溶导电情况固体不导电,熔化或溶于水后导电不导电(除硅)一般不导电良导体一、四种晶体类型对比离子晶体原子晶体分子晶体1
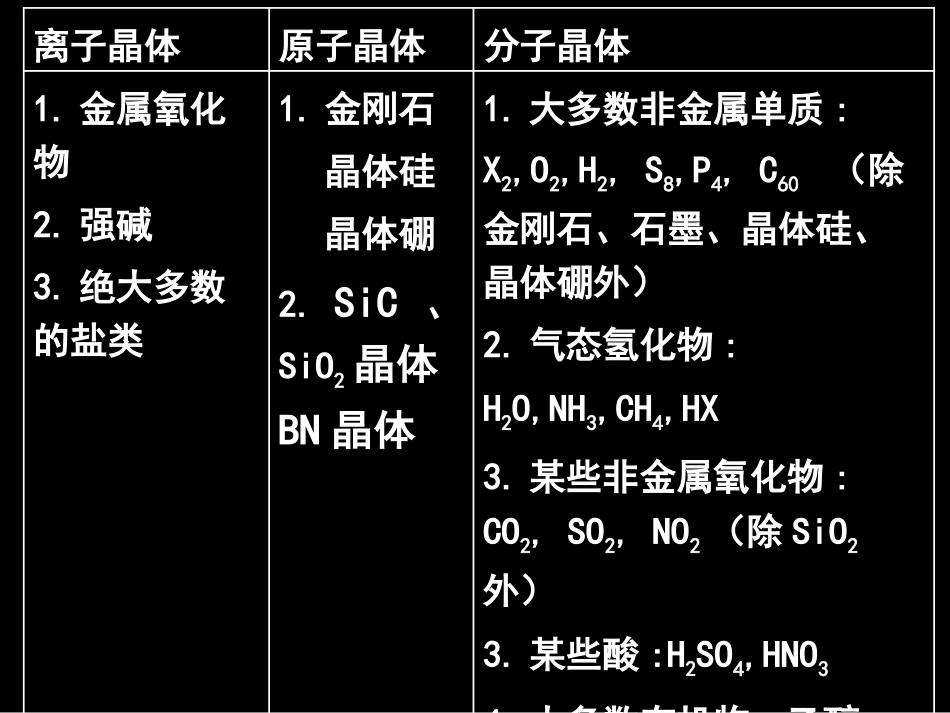
金属氧化物2
绝大多数的盐类1
金刚石晶体硅晶体硼2
SiC、SiO2晶体BN晶体1
大多数非金属单质:X2,O2,H2,S8,P4,C60(除金刚石、石墨、晶体硅、晶体硼外)2
气态氢化物:H2O,NH3,CH4,HX3
某些非金属氧化物:CO2,SO2,NO2(除SiO2外)3
某些酸:H2SO4,HNO34
大多数有机物:乙醇,蔗糖(除有机盐)(2011四川)下列说法正确的是A
分子晶体中一定存在分子间作用力,不一定存在共价键B
分子中含两个氢原子的酸一定是二元酸C
含有金属离子的晶体一定是离子晶体D
元素的非金属型越强,其单质的活泼性一定越强当堂巩固事半功倍晶体熔沸点高低的判断方法11、不同晶体类型的熔沸点比较、不同晶体类型的熔沸点比较一般:原子晶体一般:原子晶体>>离子晶体离子晶体>>分子晶体(有例分子晶体(有例外)外)氧化镁熔点2852℃二氧化硅熔点1723℃氧化铝熔点2050℃氯化铝熔点190℃氯化钠熔点801℃氯化镁熔点714℃金刚石熔点3350℃碳化硅熔点2600℃离子晶体的晶格能的大小离子间的库仑力不能简单用衡量晶体熔沸点高低的判断方法22、同种晶体类型物质的熔沸点比较、同种晶体类型物质的熔沸点比较①①离子晶体:离子晶体:阴、阳离子阴、阳离子电荷数越大,半径越小熔沸点越高熔沸点越高②②原子晶体:原子晶体:原子半径越小原子半径越小→→键长越短键长越短→→键能越大键能越大