第 1 页 共 9 页 《化学反应速率与化学平衡》高考真题训练 1.(2011·江苏·10)下列图示与对应的叙述相符的是 ( ) A.图 1 表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 B.图 2 表示 0
1000 mol·L-1NaOH 溶液滴定 20
00 mL 0
1000mol·L-1CH3COOH 溶液所得到的滴定曲线 C.图 3 表示 KNO3 的溶解度曲线,图中 a 点所示的溶液是 80℃时 KNO3 的不饱和溶液
D.图 4 表示某可逆反应生成物的量随反应时间变化的曲线,由图知 t 时反应物转化率最大 【答案】C 【解析】 “反应物总能量比生成物总能量高”为放热反应,A 错误; 醋酸是弱酸,0
1000mol·L-1CH3COOH 溶液 pH 大于 1,B 错误; 溶解度曲线上的点表示饱和溶液,在一定温度下,曲线下方的溶液要达到饱和,需增加溶质,所以 C 正确; 由图 4 可知反应从正向开始,t 时刻还未达到平衡,所以转化率未达到最大,D 错误
2.(2011·江苏·15)700℃时,向容积为 2L 的密闭容器中充入一定量的 CO 和 H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g) 反应过程中测定的部分数据见下表(表中 t2>t1): 反应时间/min n(CO)/mol n(H2O)/ mol 0 1
60 t1 0
80 t2 0
20 下列说法正确的是 ( ) A.反应在 t1 min 内的平均速率为11210
40()minv HmolLt B.保持其他条件不变,起始时向容器中充入 0
60 mol CO 和 1
20 mol H2O,到达平衡时 n(CO2)=0
40 mol
C.保持其他条件不变,向平衡体系中再通入 0
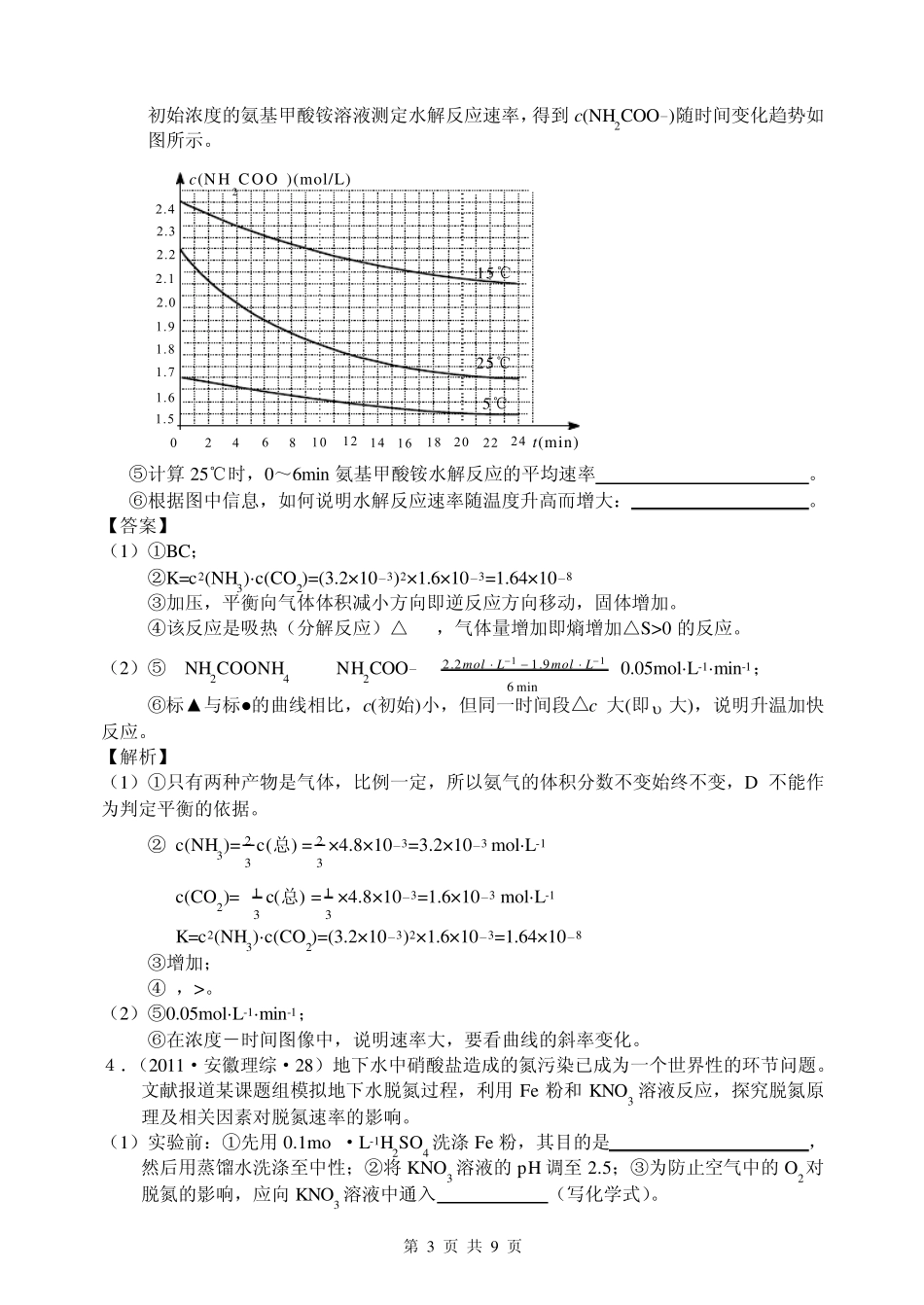
20 mol H2O,与原平衡相比,达到新平衡时 CO 转化