6g+23xl00%=10%【化学】初三化学化学计算题专项训练及答案一、中考化学计算题1
6gNaCl 和 MgCb 固体混合物完全溶于 126g 水中配成溶液,再将 200g-*定溶质质量分数的NaOH 溶液不断加入该溶液中
充分反应后,测得的实验数据如卞表
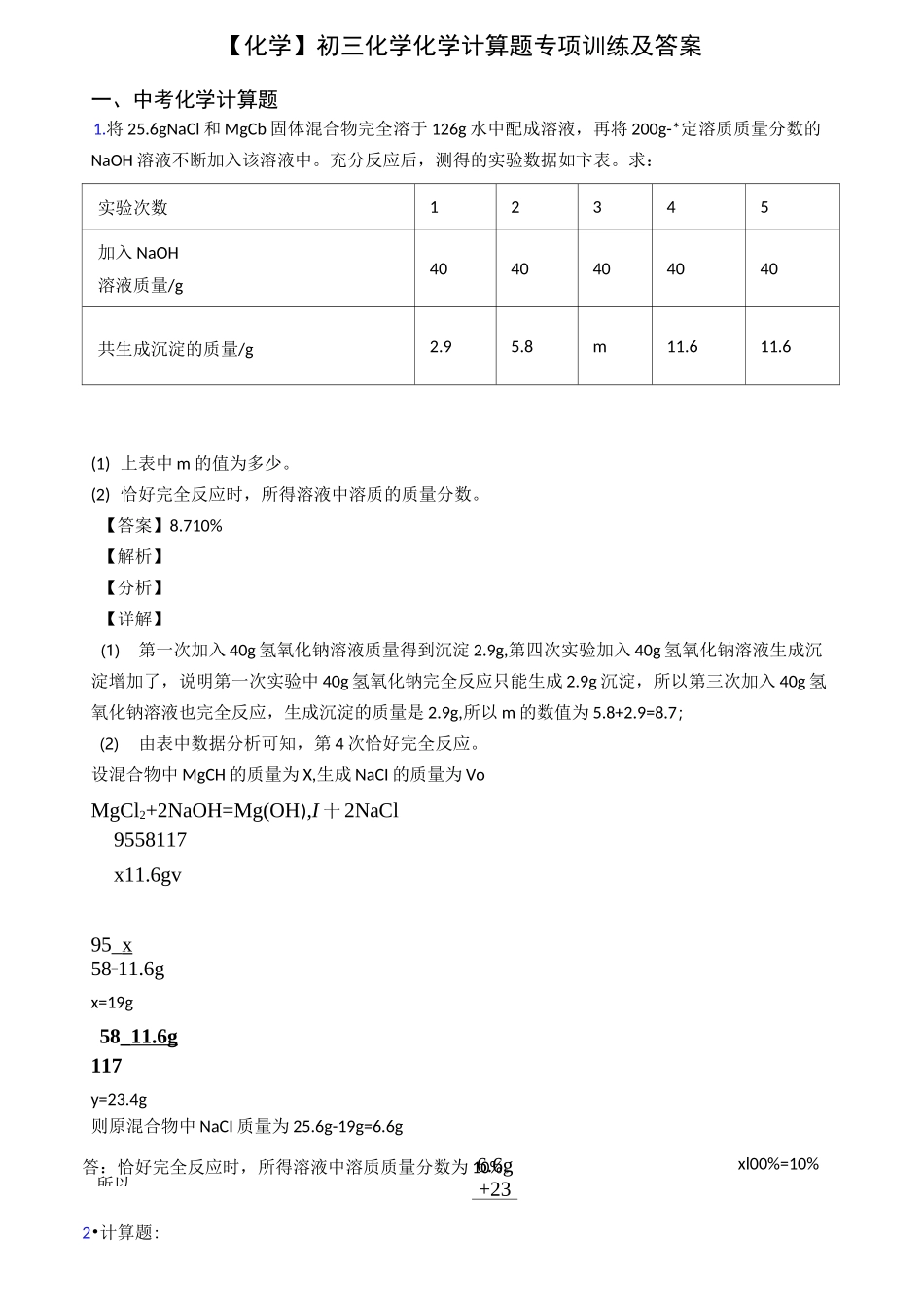
求:实验次数12345加入 NaOH溶液质量/g4040404040共生成沉淀的质量/g2
6(1) 上表中 m 的值为多少
(2) 恰好完全反应时,所得溶液中溶质的质量分数
710%【解析】【分析】【详解】(1)第一次加入 40g 氢氧化钠溶液质量得到沉淀 2
9g,第四次实验加入 40g 氢氧化钠溶液生成沉淀增加了,说明第一次实验中 40g 氢氧化钠完全反应只能生成 2
9g 沉淀,所以第三次加入 40g 氢氧化钠溶液也完全反应,生成沉淀的质量是 2
9g,所以 m 的数值为 5
7;(2)由表中数据分析可知,第 4 次恰好完全反应
设混合物中 MgCH 的质量为 X,生成 NaCI 的质量为 VoMgCl2+2NaOH=Mg(OH),I 十 2NaCl9558117x11
6gv95_x58_11
6gx=19g58_11
6g117y=23
4g则原混合物中 NaCI 质量为 25
6g-19g=6
6g答:恰好完全反应时,所得溶液中溶质质量分数为 10%
2•计算题:某固体样品可能含有 NaCl、NaHg、NafOs 中的一种、二种或三种
某兴趣小组取出 100g 固体与足量的桶硫酸反应,将产生的气体通入足量的澄清石灰水,生成沉淀 100go 然后又取出等质量的样品加水溶解,再加入足量的 CaCl:生成沉淀 50g(d^:NaHC03与 CaCl:不反应)
(1) 该固体样品成分是 o(2) 求该固体样品中 Sg 质量分数为多少