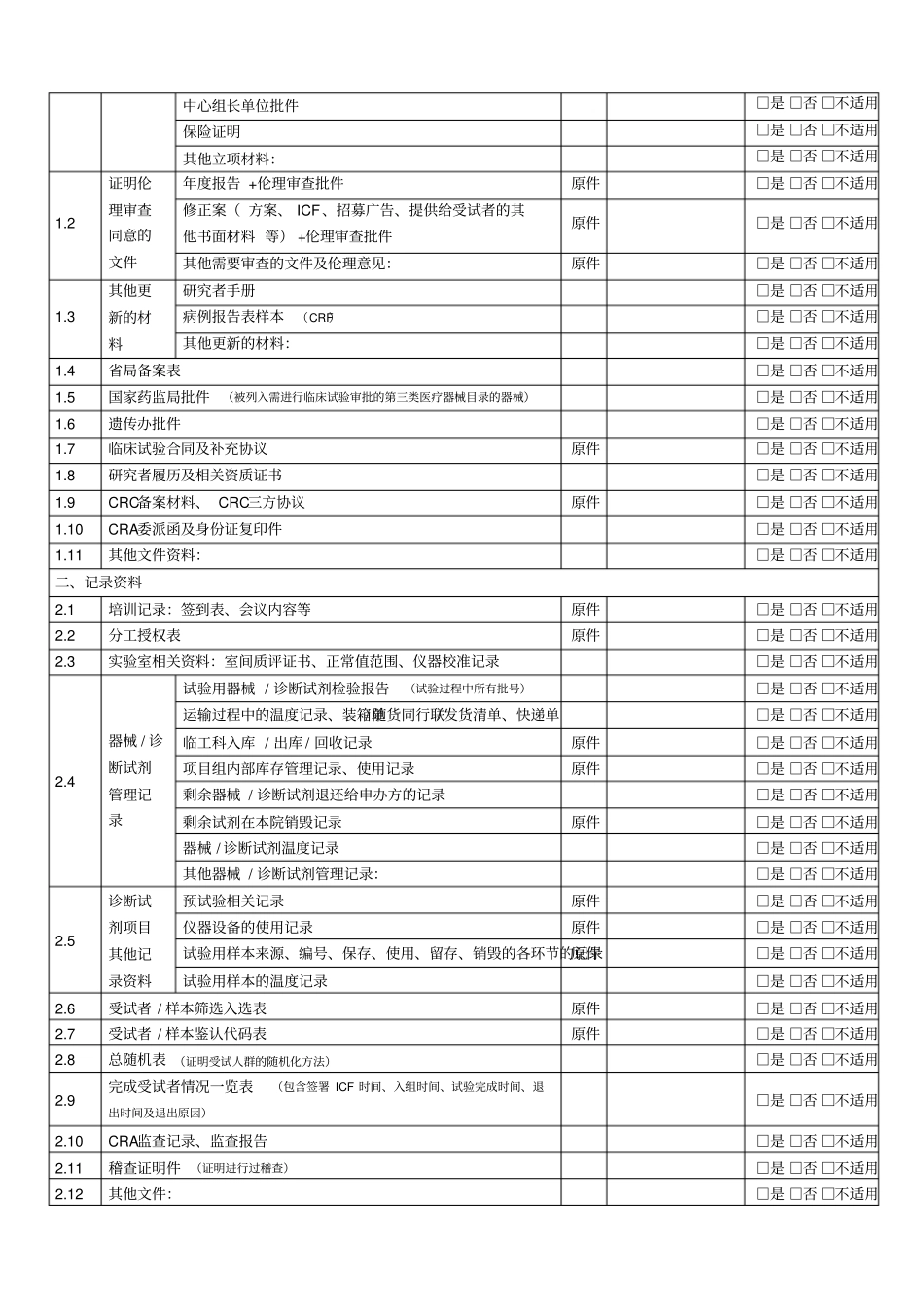
邵逸夫医院器械临床试验资料存档交接单申办单位:(CRO):承担科室:项目名称及方案编号:(编号:)临床试验保存期限:保存年,年月日 —年月日资料到期后联系人及联系方式一:资料到期后联系人及联系方式二:序号归档材料名称要求备注是否完整一、文件资料1
1 立项材料首次通过伦理审查的批件原件□是 □否 □不适用器械临床试验申请表原件□是 □否 □不适用初始审查申请表原件□是 □否 □不适用研究者利益冲突声明原件□是 □否 □不适用申办者营业执照□是 □否 □不适用医疗器械生产企业许可证□是 □否 □不适用CRO营业执照、申办方与CRO的委托书□是 □否 □不适用适用的技术要求/ 注册产品标准 / 相关国家行业标准□是 □否 □不适用自检合格报告□是 □否 □不适用具有资质的检验机构出具的一年内的产品注册检验合格报告□是 □否 □不适用临床试验方案原件□是 □否 □不适用研究者手册 / 临床试验须知□是 □否 □不适用产品的动物试验报告(用于植入人体的医疗器械)□是 □否 □不适用知情同意书文本和其他提供给受试者的书面材料□是 □否 □不适用招募受试者和向其宣传的程序性文件□是 □否 □不适用免知情同意的申请原件□是 □否 □不适用病例报告表文本□是 □否 □不适用临床试验机构的设施条件能够满足试验的综述原件□是 □否 □不适用研究者履历及相关资质证明□是 □否 □不适用试验用医疗器械的研制符合适用的医疗器械质量管理体系相关要求的声明□是 □否 □不适用申办者保证所提供资料真实性的声明原件□是 □否 □不适用研究者保证所提供资料真实性的声明原件□是 □否 □不适用医疗器械严重不良事件报告表样本□是 □否 □不适用破盲规程□是 □否 □不适用试验用医疗器械标签□是 □否 □不适用临床研究原始记录样本□是 □否 □不适用医疗器械临床试验实施者诚信承诺书原件□是 □否 □不适用申办方责任