复习上一次课内容复习上一次课内容一、溶解度在一定的温度下,某溶质在一定量的溶剂中溶解达平衡时溶解的量称为溶解度
对于微溶化合物,也有溶解,难溶物质通常用“s”表示溶解度
表示达到平衡时每升溶液中溶质B的物质的量
单位molL-1
•微溶物在水中的溶解和电离是分步进行的:•MA(s)===MA(aq,s0)===M++A–•式中s0是在一定的温度下MA的溶解度
aq表示以水做溶剂的溶液(即水溶液)•在一定的温度下s0为一常数,称为该物质的固有溶解度或分子溶解度(单位:)
1molL1molL1molL•二、溶度积•氯化银虽然是难溶物,如果把它的晶体放入水中,或多或少仍有所溶解,可表示为:•标准平衡常数表达式为:•••Ksp(AgCl)==[Ag+]×[Cl-]=SS=S2•称为该微溶化合物的溶度积常数,简称为溶度积
•溶度积常数仅使用于难溶电解质的饱和溶液,对中等或易溶电解质不适用
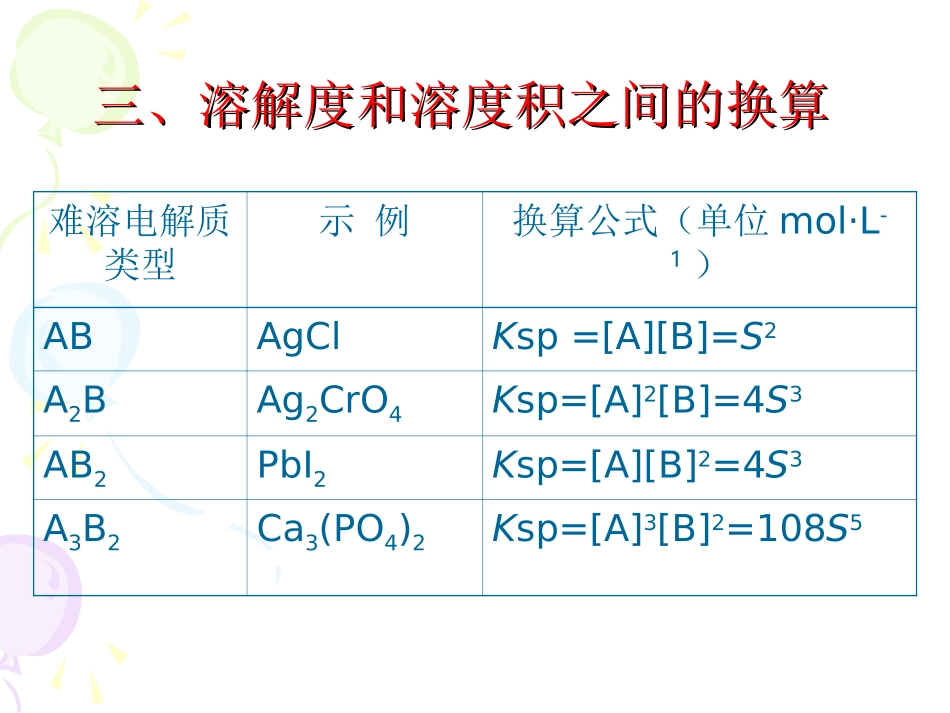
()AgClsAgCl溶解沉淀()()()'()'()()SPcAgcClKAgClcAgcClcAgCl[AgCl]]-][Cl[Ag三、溶解度和溶度积之间的换算三、溶解度和溶度积之间的换算难溶电解质类型示例换算公式(单位mol·L-1)ABAgClKsp=[A][B]=S2A2BAg2CrO4Ksp=[A]2[B]=4S3AB2PbI2Ksp=[A][B]2=4S3A3B2Ca3(PO4)2Ksp=[A]3[B]2=108S5•实例25℃时CaF2的Ksp=2
710-11,求饱和溶液中Ca2+、F-的浓度以及CaF2在水中的溶解度
•解:CaF2(s)=Ca2+(aq)+2F-(aq)•S2S•[Ca2+]=S[F-]=2S•Ksp(CaF2)=[Ca2+][F-]2=[S][2S]2=4S3•则溶解度S=1