风险管理控制程序1
0 目的通过对公司所有设计和生产的医疗器械在其寿命期内的各个阶段的风险因素及水平进行分析,采用适宜的管理方法控制和降低风险水平
0 范围适用于本公司设计和生产的医疗器械在其寿命期内的各个阶段的风险管理
1 技术部:a
负责编制《风险管理计划》,并按计划和《风险管理控制程序》规定的内容和要求对风险实施管理和控制
负责根据产品在设计开发阶段组建风险管理小组,建立产品风险管理档案
风险管理小组成员负责编制风险管理过程中的文件和记录,项目负责人负责审核风险管理过程中的文件和记录
技术部经理负责批准风险管理过程中的文件和记录,并向总经理报告风险管理和评价的结果
2 办公室(质量体系管理部门):a
负责各部门之间与风险管理有关的资料和信息的传递
负责风险管理过程控制的监督、检查和评审
3 各部门:参与评价风险水平,实施与本部门有关的风险管理各项方案,监控实施的有效性
4 销售部:负责收集产品销售后的风险信息,并及时反馈或传递至办公室
5 总经理a
负责风险管理所需资源的提供,包括人员资格、必要的培训、信息获取、研究试验所需经费等
负责风险可接受准则方针的确定
按计划的间隔保持对风险管理的评审
0 工作程序4
1 人员资格:所有从事风险管理工作的执行者应具有和赋予他们的任务相适应医疗器械及其应用的北京神鹿医疗器械有限公司风险管理控制程序章节号版本/修订页次7
0-2D/05/知识和经验,以及具有风险管理技术知识
必要时应培训
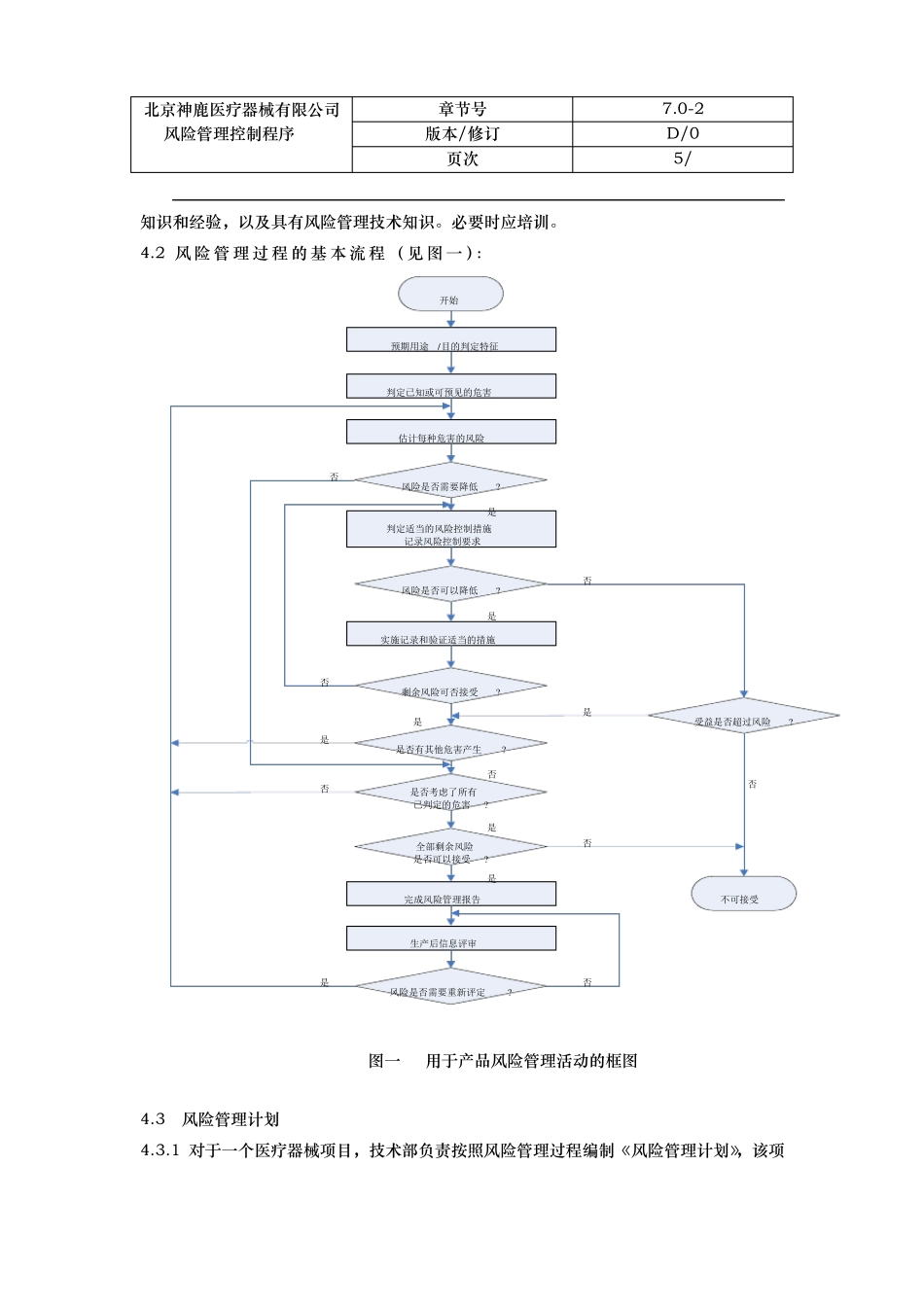
2 风 险 管 理 过 程 的 基 本 流 程 ( 见 图 一 ):开始预期用途/目的判定特征判定已知或可预见的危害估计每种危害的风险否风险是否需要降低
是判定适当的风险控制措施记录风险控制要求否风险是否可以降低
是实施记录和验证适当的措施否剩余风险可否接受
是是是是否有