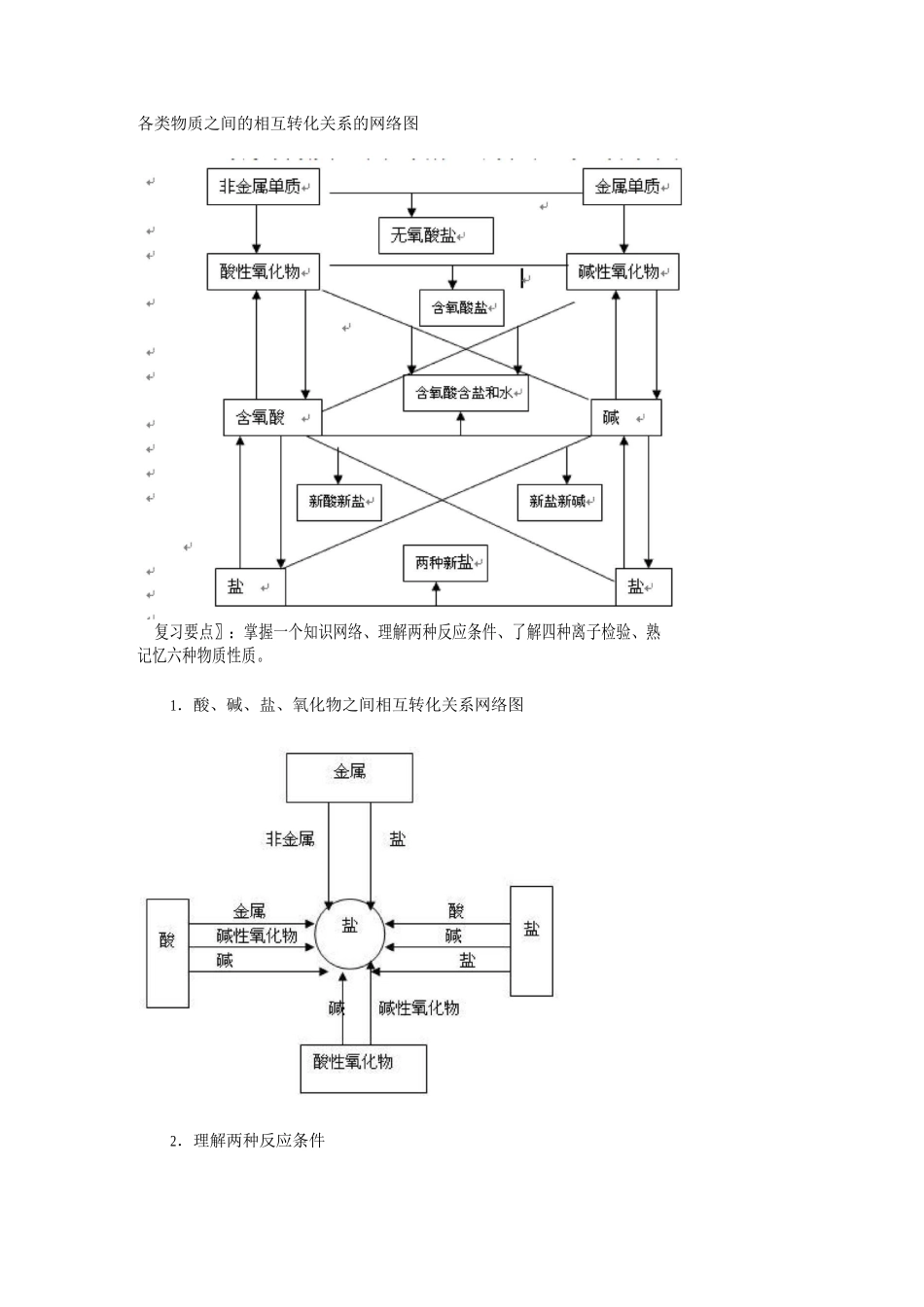
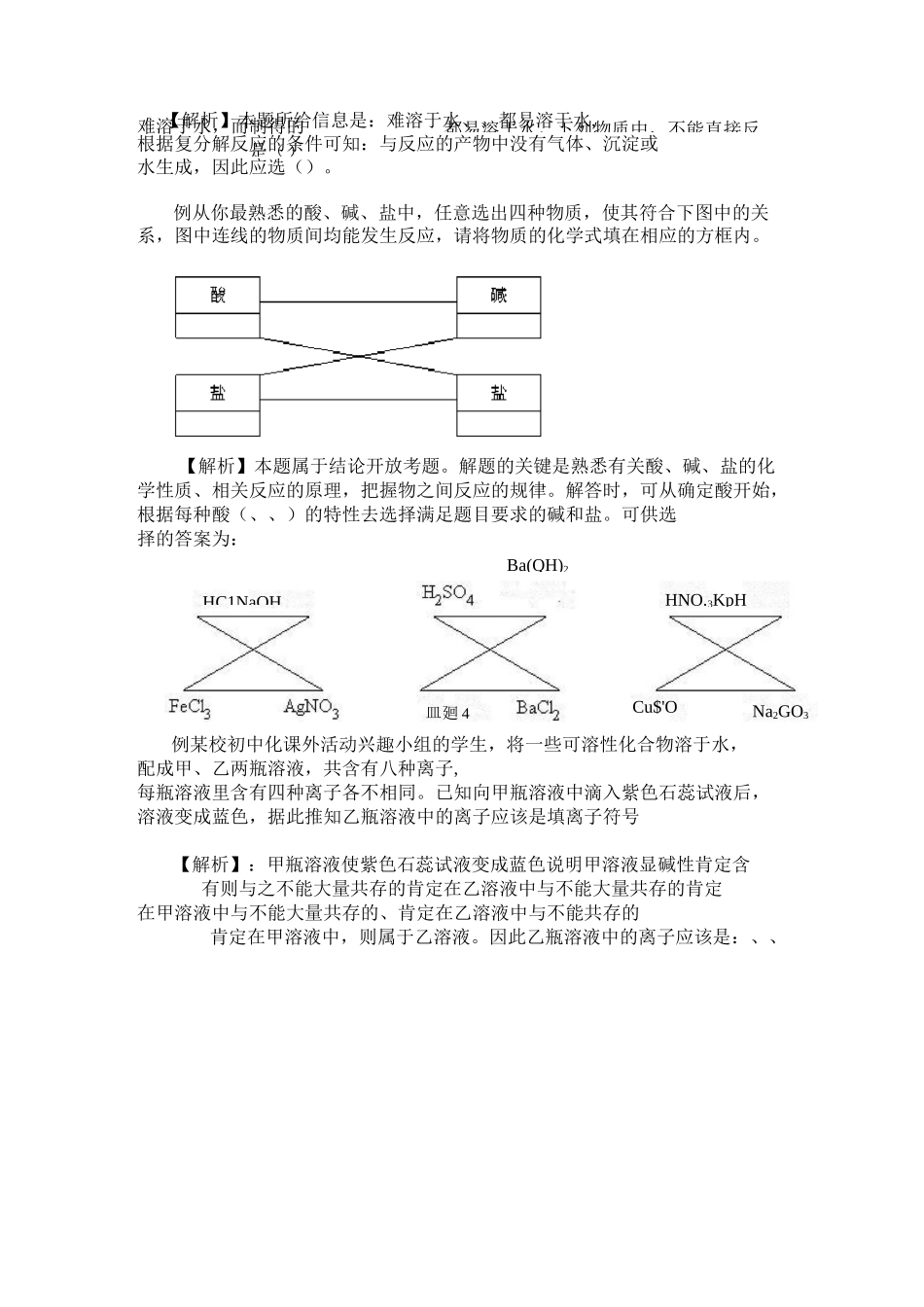
各类物质之间的相互转化关系的网络图复习要点〗:掌握一个知识网络、理解两种反应条件、了解四种离子检验、熟记忆六种物质性质
1.酸、碱、盐、氧化物之间相互转化关系网络图2.理解两种反应条件复分解反应发生的条件:(1)从定以上分析:复分解反应是两种化合物相互交换成份生成另外两种化合物的反应
判断一个反应是否是复分解反应不能仅仅依据反应物和生成物的种类来判断,还必须看反应的实质
如:2NaOH+CO2=Na2CO3+H2O 就不属于复分解反应,因为两种反应物没有相互交换成份
再如:CaCO3+2HCl=CaCl2+H2O+CO2T,从形式上来看,虽然该反应的产物有三种化合物生成,但却属于复分解反应,该反应的实质是:CaCO3+2HCl=CaCl2+H2CO3,H2CO3不稳定分解为 H2O 和 C02,因此该却反应属于复分解反应
(2)复分解反应发生的条件是:①对于反应物来说:酸与碱反应,二者至少有一种要溶于水;酸与盐反应是酸必须溶于水;盐与碱、盐与盐反应时,两种反应物必须全部溶于水
②对于生成物来说要么有水生成,要么有沉淀生成,要么有气体生成
金属与盐溶液发生置换反应的条件:金属与盐溶液发生置换反应的条件是金属的位置:只有排在前面的金属才能把后面的金属从其盐溶液中置换出来;特殊性:由于钾、钙、钠的化学性质非常活泼,在盐溶液中它们会首先与水反应生成相应的碱和氢气,因而不会置换出盐中的金属;盐必须溶于水
铁与盐溶液反应时生成价的亚铁盐金属与铁盐反应时,要用价的亚铁盐
3.四种离子的检验检验方法()SO 的检验 Ba 和 HNO-BaSO(白色沉淀)()Cl 的检验:AgNO 和 HNO-AgCl(白色沉淀)()NH 的检验:OH-NH-湿润的红色石蕊试纸由红色变蓝色()CO 的检验:HCl-CO-澄清的石灰水变浑浊.熟记六种物质复习时,应重点记忆三类物质的典型代表物的物理性质、化学性